J J Thomson Atomic Model – Postulates, Limitations
Όλοι πρέπει να έχετε δει στην καθημερινότητά σας ένα καρπούζι, μια σταφίδα και μια πουτίγκα δαμάσκηνου. Ένα από τα πρώιμα μοντέλα ατόμων, που ονομάζεται ατομικό μοντέλο Thomson, έχει συγκριθεί με αυτά τα τρόφιμα όσον αφορά την εμφάνιση. Αυτό το άρθρο έχει ως στόχο να συζητήσει λεπτομερώς αυτό το ατομικό μοντέλο Thomson.
Ιστορικό
Πριν ανακαλυφθούν τα υποατομικά σωματίδια, η ατομική θεωρία του Dalton δόθηκε από τον John Dalton. Σε αυτή τη θεωρία, περιέγραψε τα άτομα ως αδιαίρετα σωματίδια, πράγμα που σημαίνει ότι δεν μπορούν να διασπαστούν σε περαιτέρω μικρότερα σωματίδια. Αργότερα, τα αξιώματα που προτάθηκαν στην Ατομική Θεωρία του Dalton απορρίφθηκαν λόγω της ανακάλυψης των υποατομικών σωματιδίων από τον JJ Thomson.
Λόγω της ανακάλυψης των υποατομικών σωματιδίων από τον JJ Thomson, ξεκίνησε η αναζήτηση για το πώς αυτά είναι διατεταγμένα σε ένα άτομο. Από τους πολλούς επιστήμονες που πρότειναν μοντέλα για την ατομική δομή, ο J.J. Ο Τόμσον ήταν ο πρώτος. Το 1897, ανακάλυψε αρνητικά φορτισμένα σωματίδια μέσω ενός πειράματος που ονομάζεται πείραμα καθοδικού σωλήνα. Το όνομα «ηλεκτρόνια» δόθηκε σε αυτά τα σωματίδια. Σύμφωνα με τον J.J. Thomson, τα ηλεκτρόνια είναι 2.000 φορές ελαφρύτερα από ένα πρωτόνιο. Πίστευε επίσης ότι ένα άτομο περιλαμβάνει ένα νέφος αρνητικά φορτισμένων σωματιδίων σε μια σφαίρα θετικών φορτίων. Rutherford και J.J. Ο Thomson έδειξε για πρώτη φορά πώς ο αέρας ιονίζεται στις ακτίνες Χ.
Το μοντέλο του ατόμου του Thomson
Από τα πολλά επιστημονικά μοντέλα ενός ατόμου, το ατομικό μοντέλο Thomson είναι αυτό που μπορούμε να συγκρίνουμε με ένα καρπούζι σε εμφάνιση. Αυτό οφείλεται στο γεγονός ότι υποδηλώνει ότι τα ηλεκτρόνια είναι διασκορπισμένα σε μια θετικά φορτισμένη σφαίρα στο άτομο όπως ακριβώς οι μαύροι σπόροι διασκορπίζονται στο κόκκινο βρώσιμο μέρος ενός καρπουζιού. Αυτό το μοντέλο δόθηκε το 1903 από τον J.J. Thomson αφού ανακάλυψε τα ηλεκτρόνια. Εκείνη την εποχή, ο πυρήνας ενός ατόμου δεν είχε ανακαλυφθεί. Ως εκ τούτου, πρότεινε ένα μοντέλο βασισμένο στις ιδιότητες των ατόμων που ήταν γνωστές εκείνη την εποχή. Αυτά ήταν:
- Τα άτομα φέρουν ουδέτερο φορτίο. Δεν είναι ούτε θετικά ούτε αρνητικά φορτισμένα καθώς οι δύο τύποι φορτίων μέσα τους ισορροπούν μεταξύ τους.
- Ένα άτομο αποτελείται από αρνητικά φορτισμένα σωματίδια γνωστά ως ηλεκτρόνια.
Αποθέσεις του Ατομικού Μοντέλου του Τόμσον
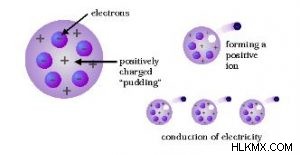
Σύμφωνα με αυτά τα αξιώματα του Ατομικού Μοντέλου του Thomson, ένα άτομο μοιάζει με μια σφαίρα θετικού φορτίου που περιέχει αρνητικά φορτισμένα σωματίδια που ονομάζονται ηλεκτρόνια. Καθώς το μέγεθος των αρνητικά φορτισμένων σωματιδίων και του θετικού φορτίου είναι ίσο, εξισορροπούν το ένα το άλλο και, επομένως, το άτομο είναι ηλεκτρικά ουδέτερο ως σύνολο, χωρίς φορτίο.
Το ατομικό μοντέλο που προτείνει ο Thomson μοιάζει με καρπούζι ή σφαιρική πουτίγκα δαμάσκηνου. Αυτό συμβαίνει επειδή, σε αυτό το μοντέλο, τα ηλεκτρόνια μοιάζουν με σταφίδες ενσωματωμένες σε μια σφαίρα θετικού φορτίου, όπως ακριβώς φαίνεται μια πουτίγκα δαμάσκηνου. Μοιάζει επίσης με καρπούζι καθώς το κόκκινο βρώσιμο μέρος του καρπού μπορεί να συγκριθεί με τη θετικά φορτισμένη σφαίρα, ενώ οι μαύροι σπόροι που είναι διασκορπισμένοι στον καρπό μοιάζουν με τα ηλεκτρόνια της σφαίρας.

Εργασία στο Ατομικό Μοντέλο του Thomson
Μια σειρά πειραμάτων διεξήχθη από τον J.J. Thomson για να παρατηρήσει τη φύση των καθοδικών ακτίνων. Ο στόχος ήταν να συμπεράνουμε ότι οι καθοδικές ακτίνες είναι αρνητικά φορτισμένες. Η συσκευή που σχεδίασε ήταν γνωστή ως Καθοδικός σωλήνας. Σήμερα, ονομάζεται επίσης «Ηλεκτρονικό Πυροβόλο».
Τα ηλεκτρόνια ταξιδεύουν από την κάθοδο που βρίσκεται στην αριστερή πλευρά του σωλήνα στη φωσφορίζουσα οθόνη στη δεξιά πλευρά μέσω της ανόδου. Παρατήρησε ότι εάν το μαγνητικό πεδίο είναι απενεργοποιημένο, το ηλεκτρικό πεδίο μπορεί να εκτρέψει τη δέσμη. Παρατήρησε επίσης ότι αν προσαρμόζαμε τις εντάσεις των μαγνητικών και ηλεκτρικών πεδίων, δεν παρατηρήθηκε καμία απόκλιση στις καθοδικές ακτίνες.
Εάν η πίεση είναι χαμηλή (περίπου 1 mm υδραργύρου), οι καθοδικές ακτίνες φαίνονται σκοτεινές και ελαφρώς αποκλίνουσες κοντά στην κάθοδο. Η εξάπλωση αυτού του σκοτεινού χώρου συμβαίνει μέσω του σωλήνα μέχρι να φαίνεται ασαφής. Φτάνοντας στο γυαλί ή αγγίζοντας τη φωσφορίζουσα οθόνη, φαίνεται λαμπερό καθώς οι καθοδικές ακτίνες απορροφούν ενέργεια. Έκανε μετρήσεις του μήκους της συσκευής, της παραμόρφωσης και της ισχύος των μαγνητικών και ηλεκτρικών πεδίων για τον υπολογισμό του λόγου φορτίου προς μάζα. Έκανε μια παρατήρηση ότι αυτή η αναλογία δεν εξαρτιόταν από το μέταλλο και το αέριο μέσα στον σωλήνα. Αυτό τον έκανε να καταλήξει στο συμπέρασμα ότι αυτά τα αρνητικά φορτισμένα σωματίδια ήταν ατομικά σωματίδια.
Παρατήρησε ότι όταν εφαρμόζουμε ένα ομοιόμορφο μαγνητικό πεδίο με ισχύ Β σε κατεύθυνση κάθετη προς αυτή της κίνησης των φορτισμένων σωματιδίων, αυτά εκτρέπονται σε μια κυκλική διαδρομή. Μπορούμε να λάβουμε την ακτίνα R αυτής της κυκλικής διαδρομής διατηρώντας το μαγνητικό πεδίο «qvB» ίσο με τη μάζα επί την κεντρομόλο επιτάχυνση. Σε μεταγενέστερα πειράματα, ο Thomson άλλαξε τα μαγνητικά και ηλεκτρικά πεδία με τρόπο ώστε η δέσμη της καθόδου να μην εκτρέπεται. μάλλον, θα ήταν ίσιο. Κάνοντας ίσες τις μαγνητικές και τις ηλεκτρικές δυνάμεις, θα μπορούσε να ανακαλύψει την ταχύτητα v.
Εφαρμογές του μοντέλου Plum Pudding
- Το πείραμα της Καθοδικής Ακτίνας από τον J.J. Ο Thomson άνοιξε τον δρόμο για τα σύγχρονα ηλεκτρονικά και αποτέλεσε τη βάση της ανακάλυψης διόδων και τρανζίστορ. Οι ερευνητές κατέληξαν στο συμπέρασμα από τα πειράματα ότι οι καθοδικές ακτίνες διαδίδονται σε ευθεία γραμμή και τους βοήθησαν στη μελέτη των ιδιοτήτων των κυμάτων.
- Οι λυχνίες καθοδικών ακτίνων χρησιμοποιούνται ευρέως στις ηλεκτρονικές συσκευές στις μέρες μας.
- Τα πειράματα που πραγματοποιήθηκαν από τον J.J. Ο Thomson οδήγησε στην επανάσταση στη σύγχρονη Κβαντική Φυσική.
Περιορισμοί του ατομικού μοντέλου Thomson
- Το ατομικό του μοντέλο δεν ήταν σε θέση να περιγράψει πώς ένα θετικό φορτίο συγκρατεί τα αρνητικά φορτισμένα ηλεκτρόνια σε ένα άτομο, γεγονός που το εμπόδισε να εξηγώντας τη σταθερότητα ενός ατόμου. Ως αποτέλεσμα, αυτή η υπόθεση δεν ήταν σε θέση να εξηγήσει τη θέση του πυρήνα ενός ατόμου.
- Το μοντέλο του Thomson δεν ήταν σε θέση να εξηγήσει πώς τα λεπτά μεταλλικά φύλλα διασκορπίζουν τα σωματίδια άλφα.
- Δεν υπάρχει πειραματική απόδειξη για το αντίθετο.
Αν και το μοντέλο του Thomson δεν αντιπροσώπευε με ακρίβεια την ατομική δομή, χρησίμευσε ως το θεμέλιο για τη δημιουργία διαφόρων ατομικών μοντέλων. Βρείτε το pdf της ατομικής δομής εδώ. Πολυάριθμες τεχνολογίες που έχουν συμβάλει σημαντικά στην πρόοδο της ανθρωπότητας κατέστησαν δυνατές με την έρευνα για το άτομο και τη δομή του.
Άλλα ατομικά μοντέλα
Ατομικό μοντέλο του Ράδερφορντ
Καθώς το μοντέλο της πουτίγκας δαμάσκηνου απέτυχε να εξηγήσει ορισμένες πτυχές της ατομικής δομής, ένας Βρετανός επιστήμονας ονόματι Ernest Rutherford πραγματοποίησε ένα πείραμα. Με βάση τις παρατηρήσεις που έκανε σε αυτό το πείραμα, έδωσε το δικό του ατομικό μοντέλο. Σύμφωνα με τον ίδιο, το μεγαλύτερο μέρος του θετικού φορτίου και της ατομικής μάζας γεμίζονται σε έναν μικρό όγκο που ονομάζεται πυρήνας. Πρότεινε επίσης τα ηλεκτρόνια να περιβάλλουν τον πυρήνα και να περιφέρονται γύρω του σε κυκλικές διαδρομές. Καθώς ο πυρήνας θεωρήθηκε ότι είναι μια πυκνά συγκεντρωμένη μάζα θετικού φορτίου και τα ηλεκτρόνια που περιστρέφονται γύρω από αυτόν είναι αρνητικά φορτισμένα, συγκρατούνται μεταξύ τους από ισχυρές δυνάμεις έλξης που ονομάζονται ηλεκτροστατικές δυνάμεις.
Ατομικό μοντέλο του Bohr
Ο Neil Bohr έδωσε το ατομικό του μοντέλο το 1915 ως τροποποίηση του ατομικού μοντέλου του Rutherford. Όπως συζητήθηκε παραπάνω, ο Rutherford πρότεινε ότι το άτομο περιέχει έναν πυρήνα που είναι συγκεντρωμένος με θετικό φορτίο και περιβάλλεται από αρνητικά φορτισμένα ηλεκτρόνια που περιστρέφονται γύρω του σε κυκλικές διαδρομές που ονομάζονται τροχιές. Ο Bohr ονόμασε αυτές τις τροχιές τροχιακά κελύφη και πρότεινε ότι κάθε τροχιά έχει μια σταθερή ποσότητα ενέργειας, της οποίας τα διαφορετικά επίπεδα αντιπροσωπεύονται από 1,2,3 κ.λπ., που ονομάζονται κβαντικοί αριθμοί. Η αρίθμηση ξεκινά από τον πυρήνα, με το n=1 να θεωρείται το χαμηλότερο επίπεδο ενέργειας. Τα επόμενα τροχιακά κελύφη ορίζονται ως K, L, M…. ούτω καθεξής με n=1,2,3….. ούτω καθεξής. Ένα ηλεκτρόνιο θεωρείται στη θεμελιώδη κατάσταση όταν το ενεργειακό του επίπεδο είναι το χαμηλότερο.
Σε ένα άτομο, τα ηλεκτρόνια αποκτούν ένα ορισμένο ποσό ενέργειας και ταξιδεύουν σε ένα υψηλότερο επίπεδο ενέργειας από ένα χαμηλότερο επίπεδο ενέργειας. Εάν χαθεί ενέργεια, τα ηλεκτρόνια ταξιδεύουν σε χαμηλότερο επίπεδο ενέργειας από υψηλότερο επίπεδο ενέργειας.
Συμπέρασμα
Αν και η ανακάλυψη του JJ Thomson του ατομικού μοντέλου δεν ισχύει στις μέρες μας και έχει περιορισμούς, άνοιξε το δρόμο για πολλά άλλα μοντέλα ατομικής δομής που ήρθαν στο φως αργότερα. Χρησιμοποίησε ως μοντέλο θεμελίωσης που έδωσε τη θέση του σε σημαντικές επαναστατικές εφευρέσεις στη συνέχεια.
Συχνές ερωτήσεις
1. Γιατί απορρίφθηκε η ανακάλυψη του ατομικού μοντέλου Thomson;
Α) Το ατομικό μοντέλο του Thomson δεν μπορούσε να εξηγήσει τη σταθερότητα ενός ατόμου. Επίσης, ο Thomson πρότεινε ότι τα ηλεκτρόνια κατανέμονται στο άτομο με τρόπο παρόμοιο με τον τρόπο με τον οποίο διασπείρονται οι σπόροι σε ένα καρπούζι ή οι σταφίδες σε μια πουτίγκα. Δεν μπορούσε να εξηγήσει ότι τα χαμηλά ηλεκτρόνια κρατήθηκαν μέσα στη θετικά φορτισμένη σφαίρα. Επομένως, απορρίφθηκε.
2. Δώστε τα σημαντικά χαρακτηριστικά της ανακάλυψης Thomson του ατομικού μοντέλου.
Α) Η ανακάλυψη Thomson του ατομικού μοντέλου είχε τα ακόλουθα χαρακτηριστικά:
- Ένα άτομο αποτελείται από μια σφαίρα θετικού φορτίου στην οποία διασκορπίζονται τα ηλεκτρόνια.
- Η ποσότητα του θετικού και του αρνητικού σε ένα άτομο είναι ίση, λόγω του οποίου είναι ηλεκτρικά ουδέτερο.
3. Με ποιο φρούτο είναι το μοντέλο της Thomson;
Α) Το ατομικό μοντέλο που έδωσε ο Thomson συγκρίνεται με ένα καρπούζι με το κόκκινο βρώσιμο μέρος να μοιάζει με θετικά φορτισμένη σφαίρα, ενώ οι μαύροι σπόροι διασκορπισμένοι σε αυτό 333 σε σύγκριση με τα ηλεκτρόνια μέσα στη σφαίρα.
4. Τι δεν εξηγήθηκε από το ατομικό μοντέλο του Thomson;
Α) Το ατομικό μοντέλο του Thomson δεν εξηγούσε τη σταθερότητα ενός ατόμου. Επίσης, δεν ανέφερε τίποτα για τα πρωτόνια και τα νετρόνια, τα νετρόνια ή τον πυρήνα.