Γιατί ένα ψάρι του γλυκού νερού δεν μπορεί να επιβιώσει στο αλμυρό νερό
Τα ψάρια του γλυκού νερού είναι ψάρια που περνούν μέρος ή όλη τη ζωή τους σε γλυκό νερό, με αλατότητα μικρότερη από 0,05%. Τα ψάρια του γλυκού νερού είναι υποτονικά για το αλμυρό νερό. Ως εκ τούτου, έχουν χαμηλή συγκέντρωση ιόντων στα κύτταρα του σώματός τους από το αλμυρό νερό. Όταν μετακινούν το αλμυρό νερό, το σωματικό νερό των ψαριών του γλυκού νερού απομακρύνεται από το σώμα, καθιστώντας τα ψάρια αφυδατωμένα και προκαλώντας το θάνατό τους. Επομένως, η διαφορά ωσμωτικότητας είναι ο κύριος λόγος για τον οποίο ένα ψάρι γλυκού νερού δεν μπορεί να επιβιώσει στο αλμυρό νερό.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η ωσμωτικότητα
– Ορισμός, Γεγονότα, Τονικότητα
2. Γιατί ένα ψάρι του γλυκού νερού δεν μπορεί να επιβιώσει στο αλμυρό νερό
– Διαδρομή όσμωσης
Βασικοί όροι:Υπερτονικά διαλύματα, υποτονικά διαλύματα, ωσμωτικότητα, όσμωση, αλμυρό νερό, τονικότητα

Τι είναι η ωσμωτικότητα
Οσμωτικότητα είναι το μέτρο της συγκέντρωσης διαλυμένης ουσίας ενός συγκεκριμένου διαλύματος. Η ωσμωτικότητα του πλάσματος είναι το μέτρο της ισορροπίας ηλεκτρολύτη-νερού του σώματος. Είναι ανάλογο με τον αριθμό των σωματιδίων ανά κιλό διαλύτη. Επομένως, τα διαλύματα με διαφορετική ωσμωτικότητα έχουν διαφορετικές συγκεντρώσεις ιόντων. Η παθητική διάχυση των μορίων του νερού συμβαίνει μεταξύ διαλυμάτων με διαφορετική ωσμωτικότητα, σε μια ημιπερατή μεμβράνη. Αυτό είναι γνωστό ως όσμωση. Η όσμωση φαίνεται στο σχήμα 1 .
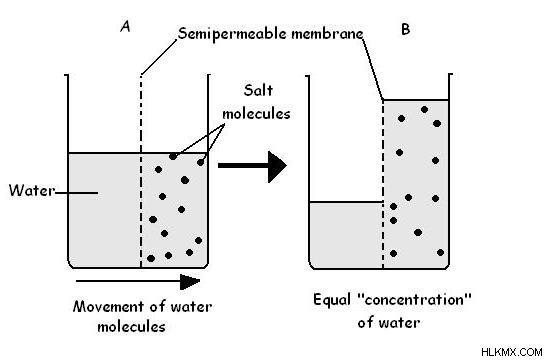
Εικόνα 1:Όσμωση
Τα διαλύματα με υψηλή συγκέντρωση ιόντων είναι γνωστά ως υπερτονικά διαλύματα ενώ τα διαλύματα με χαμηλές συγκεντρώσεις ιόντων είναι γνωστά ως υποτονικά διαλύματα. Το νερό μετακινείται από υποτονικά διαλύματα σε υπερτονικά διαλύματα. Εάν η ωσμωτικότητα δύο διαλυμάτων είναι παρόμοια, είναι γνωστά ως ισοτονικά διαλύματα. Η αποτελεσματική διαβάθμιση της οσμωτικής πίεσης είναι γνωστή ως τονικότητα.
Γιατί ένα ψάρι του γλυκού νερού δεν μπορεί να επιβιώσει στο αλμυρό νερό
Τα ψάρια του γλυκού νερού είναι ισοτονικά με το γλυκό νερό. Αυτό σημαίνει ότι τα κύτταρα του σώματός τους περιέχουν παρόμοιες συγκεντρώσεις ιόντων με το γλυκό νερό. Ωστόσο, το αλμυρό νερό περιέχει υψηλή συγκέντρωση ιόντων από το γλυκό νερό. Ως εκ τούτου, το κυτταρόπλασμα των κυττάρων του σώματος των ψαριών του γλυκού νερού είναι υποτονικό στο αλμυρό νερό. Στη συνέχεια, το νερό από το κυτταρόπλασμα μετακινείται στο αλμυρό νερό μέσω της πλασματικής μεμβράνης. Αυτή η διαδικασία συμβαίνει μέχρις ότου οι συγκεντρώσεις ιόντων του κυτταροπλάσματος και η συγκέντρωση ιόντων στο αλμυρό νερό γίνουν ίσες. Επομένως, τα ψάρια του γλυκού νερού χάνουν το νερό του σώματός τους από το αλμυρό νερό. Αυτό αφυδατώνει τα ψάρια του γλυκού νερού στο αλμυρό νερό. Ως εκ τούτου, μπορεί τελικά να πεθάνουν. Η οσμωτική ροή σε υπερτονικά διαλύματα φαίνεται στο σχήμα 2 .
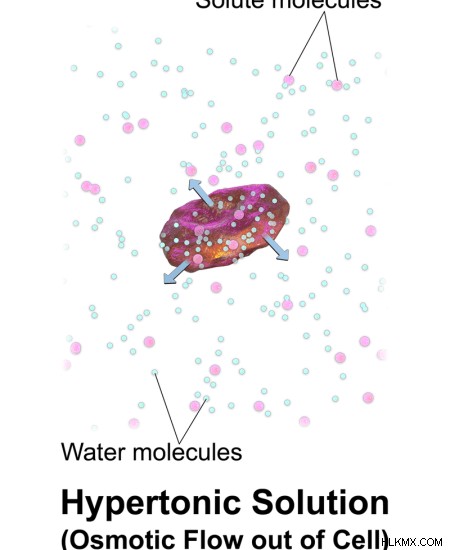
Εικόνα 2:Οσμωτική ροή σε υπερτονικά διαλύματα
Αυτό ισχύει και για τα ψάρια του αλμυρού νερού στο γλυκό νερό. Δεδομένου ότι το αλμυρό νερό περιέχει υψηλές συγκεντρώσεις ιόντων, τα σώματα των ψαριών του αλμυρού νερού περιέχουν επίσης υψηλές συγκεντρώσεις ιόντων. Όταν ένα ψάρι αλμυρού νερού ρίχνεται στο γλυκό νερό, το σώμα του ψαριού του θαλασσινού νερού είναι υπερτονικό με το γλυκό νερό. Ως εκ τούτου, το νερό κινείται στο σώμα των ψαριών του αλμυρού νερού μέσω όσμωσης, διογκώνοντας τα ψάρια του αλμυρού νερού.
Ωστόσο, ορισμένα ψάρια είναι ευρυαλονικά, δηλαδή είναι προσαρμοσμένα να ζουν τόσο σε γλυκό όσο και σε αλμυρό νερό. Έχουν μοναδικά χαρακτηριστικά ωσμορύθμισης που τους επιτρέπουν να επιβιώνουν σε διαφορετικές αλατότητες.
Συμπέρασμα
Το ψάρι του γλυκού νερού είναι υποτονικό για το αλμυρό νερό. Ως εκ τούτου, το σωματικό νερό απομακρύνεται όταν ρίχνονται στο αλμυρό νερό. Αφυδατώνονται και τελικά πεθαίνουν στο αλμυρό νερό.
Αναφορά:
1. Ωσμωση. BioNinja , Διαθέσιμο εδώ.
Εικόνα Ευγενική προσφορά:
1. «Πείραμα όσμωσης» Από τον Rlawson στα Αγγλικά Wikibooks (CC BY-SA 3.0) μέσω του Commons Wikimedia
2. “Blausen 0683 OsmoticFlow Hypertonic” Από το προσωπικό του Blausen.com (2014). «Ιατρική γκαλερί Blausen Medical 2014». WikiJournal of Medicine 1 (2). DOI:10.15347/wjm/2014.010. ISSN 2002-4436. – Δική σας εργασία (CC BY 3.0) μέσω Commons Wikimedia




