Αντιδράσεις εξουδετέρωσης οξέων βάσεων
Τι είναι η αντίδραση εξουδετέρωσης οξέων βάσεων;
Μια αντίδραση εξουδετέρωσης όξινης βάσης είναι όταν ένα οξύ αντιδρά με μια βάση για να δημιουργήσει νερό και ένα άλας.
Το πρωτόνιο (Η) από το οξύ ενώνεται με το υδροξείδιο (ΟΗ) από τη βάση για να δημιουργήσει νερό (H2 Ο). Το άλας που σχηματίζεται προέρχεται από το οξύ και τη βάση.

Αυτός ο τύπος αντίδρασης αναφέρεται ως αντίδραση εξουδετέρωσης επειδή εξουδετερώνει το οξύ και τη βάση. Εάν ένα ισχυρό οξύ και μια ισχυρή βάση αντιδράσουν πλήρως (που σημαίνει ότι υπάρχουν ίσα mol από το καθένα), τότε το διάλυμα που προκύπτει θα έχει pH 7 (ουδέτερο).
Μια αντίδραση εξουδετέρωσης είναι επίσης ένας τύπος αντίδρασης διπλής μετατόπισης.
Ποια είναι τα προϊόντα μιας αντίδρασης εξουδετέρωσης;
Τα προϊόντα μιας αντίδρασης εξουδετέρωσης θα είναι πάντα νερό (H2 Ο) και ένα αλάτι. Το αλάτι που σχηματίζεται εξαρτάται από το οξύ και τη βάση που χρησιμοποιούνται. Το άλας μπορεί να είναι διαλυτό και να διαλύεται σε διάλυμα ή μπορεί να είναι αδιάλυτο και να καταβυθίζεται εκτός διαλύματος.
Αντίδραση εξουδετέρωσης ισχυρού οξέος και ισχυρής βάσης
Η πλήρης εξουδετέρωση ενός ισχυρού οξέος και μιας ισχυρής βάσης συμβαίνει όταν υπάρχουν ίσες μοριακές ποσότητες ισχυρού οξέος και ισχυρής βάσης. Το αποτέλεσμα είναι ένα υδατικό διάλυμα που έχει pH 7.
Δεν υπάρχουν πολλά ισχυρά οξέα και ισχυρές βάσεις. Παρακάτω είναι ένας πίνακας όλων αυτών.
| Ισχυρά οξέα | Ισχυρές βάσεις |
| HCl | LiOH |
| HBr | NaOH |
| Γεια | KOH |
| HNO3 | Ca(OH)2 |
| H2 SO4 | RbOH |
| HClO3 | Sr(OH)2 |
| HClO4 | CsOH |
| Ba(OH)2 |
Εξουδετέρωση με Ασθενές Οξύ ή Ασθενή Βάση
Οι αντιδράσεις είτε με ασθενές οξύ είτε με ασθενή βάση δεν οδηγούν κανονικά σε pH 7. Νερό και αλάτι εξακολουθούν να παράγονται.
Εάν η αντίδραση περιλαμβάνει ένα ασθενές οξύ και μια ισχυρή βάση, τότε το pH που προκύπτει θα είναι ελαφρώς βασικό (pH> 7).
Όταν η αντίδραση εξουδετέρωσης περιλαμβάνει ισχυρό οξύ και ασθενή βάση, τότε το pH που προκύπτει θα είναι ελαφρώς όξινο (pH <7).
Εάν και το οξύ και η βάση είναι αδύναμα τότε το τελικό pH θα εξαρτηθεί από το pKa του οξέος και της βάσης. Το pH μπορεί να είναι όξινο, βασικό ή ουδέτερο. Αυτές οι αντιδράσεις επίσης συχνά δεν προχωρούν μέχρι την ολοκλήρωση λόγω της περιορισμένης διάστασης του ασθενούς οξέος και της ασθενούς βάσης.
| Τύπος οξέος; | Τύπος βάσης; | PH εξουδετέρωσης |
| Ισχυρό οξύ | Ισχυρή βάση | pH =7 |
| Ισχυρό οξύ | Αδύναμη βάση | pH <7 (Όξινο) |
| Ασθενές οξύ | Ισχυρή βάση | pH> 7 (Βασικό) |
| Ασθενές οξύ | Αδύναμη βάση | Εξαρτάται από το pKa και pKb |
Παράδειγμα προβλημάτων
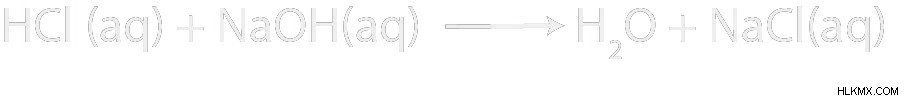
Ας υποθέσουμε ότι έχετε μια αντίδραση HCl και NaOH σε νερό. Ποια θα είναι τα προϊόντα; Τι είδους αντίδραση είναι αυτή; Και ποια είναι η καθαρή ιοντική εξίσωση;
Το HCl είναι ένα ισχυρό οξύ. Το NaOH είναι μια ισχυρή βάση. Επειδή υπάρχουν και ένα οξύ και μια βάση, γνωρίζουμε ότι έχουμε μια αντίδραση εξουδετέρωσης όξινης βάσης.
Τα προϊόντα μιας αντίδρασης εξουδετέρωσης θα είναι πάντα νερό και αλάτι. Σε αυτή την περίπτωση, το άλας μας είναι NaCl. Το ιόν νατρίου προέρχεται από την ισχυρή βάση και το ιόν χλωρίου προέρχεται από το ισχυρό οξύ.
Στη συνέχεια θέλουμε να γράψουμε την καθαρή ιοντική εξίσωση (NIE). Αρκετά από τα είδη στην αντίδρασή μας είναι υδατικά, επομένως θα πρέπει να είμαστε σε θέση να απλοποιήσουμε την εξίσωσή μας. Λαμβάνουμε την καθαρή ιοντική εξίσωση απαλλαγούμε από τυχόν ιόντα θεατών που εμφανίζονται και στις δύο πλευρές της εξίσωσης. Σε αυτήν την περίπτωση, δηλαδή Cl και Na.
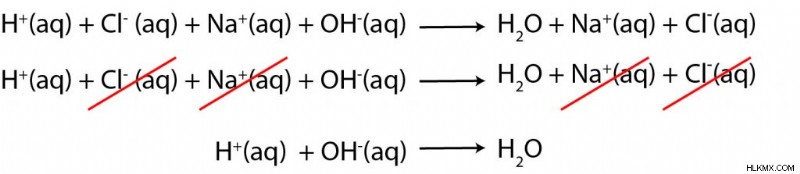
Το αποτέλεσμα είναι να έχουμε πρωτόνια (Η) από την όξινη αντίδραση με υδροξείδιο (ΟΗ) από τη βάση για να σχηματίσουμε νερό!
Παραδείγματα πραγματικής ζωής
Το μαγείρεμα χρησιμοποιεί συνήθως αντιδράσεις εξουδετέρωσης όξινων βάσεων! Για παράδειγμα, όταν ψήνουμε κέικ, προσθέτετε συχνά διττανθρακικό (μαγειρική σόδα) ως συστατικό. Η μαγειρική σόδα είναι μια βάση. Υπάρχουν και οξέα σε κάποια συστατικά! Τα κοινά είναι ο χυμός λεμονιού, το ξύδι ή η κρέμα. Όταν τα οξέα και η βάση αντιδρούν κατά το μαγείρεμα παράγουν νερό (όπως κάνουν όλες οι αντιδράσεις εξουδετέρωσης!) και διοξείδιο του άνθρακα. Οι φυσαλίδες διοξειδίου του άνθρακα είναι αυτές που κάνουν το κέικ (και άλλα αρτοσκευάσματα) αφράτο και ελαφρύ!
Για ένα πείραμα που μπορείτε να δοκιμάσετε στο σπίτι, ρίξτε μια ματιά σε αυτό το πείραμα του Science is Fun!

Άλλα σχετικά άρθρα ενδιαφέροντος
- Θεωρίες οξέων βάσεων
- Χημεία Οξέων Βάσεων
- Ιδιότητες οξέων και βάσεων