Τι θα παρατηρηθεί όταν το οξικό οξύ αντιδρά με υδροξείδιο του καλίου;
1. Σχηματισμός οξικού καλίου :
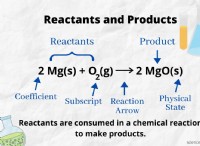
Η αντίδραση μεταξύ οξικού οξέος και υδροξειδίου του καλίου έχει ως αποτέλεσμα τον σχηματισμό οξικού καλίου (ch₃cook). Αυτό το άλας παράγεται από την ανταλλαγή ιόντων υδρογόνου (Η+) από οξικό οξύ με ιόντα καλίου (Κ+) από υδροξείδιο του καλίου.
2. Αντίδραση εξουδετέρωσης :
Το οξικό οξύ είναι ένα ασθενές οξύ και το υδροξείδιο του καλίου είναι μια ισχυρή βάση. Όταν αντιδρούν, εμφανίζεται η αντίδραση εξουδετέρωσης οξέος βάσης. Τα ιόντα υδρογόνου από οξικό οξύ συνδυάζονται με τα ιόντα υδροξειδίου (ΟΗ-) από το υδροξείδιο του καλίου για να σχηματίσουν νερό (ΗΟΟ).
3. αλλαγή pH :
Πριν από την αντίδραση, το οξικό οξύ είναι όξινο και το υδροξείδιο του καλίου είναι βασικό. Μετά την αντίδραση, το προκύπτον διάλυμα γίνεται ουδέτερο ή ελαφρώς βασικό λόγω του σχηματισμού οξικού καλίου. Αυτή η αλλαγή στο ρΗ μπορεί να παρατηρηθεί χρησιμοποιώντας ένα μετρητή pH ή με την προσθήκη ενός δείκτη όπως η φαινολοφθαλεΐνη, η οποία μετατρέπεται σε ροζ σε μια βασική λύση.
4. Απελευθέρωση θερμότητας :
Η αντίδραση εξουδετέρωσης μεταξύ οξικού οξέος και υδροξειδίου του καλίου είναι εξωθερμική, που σημαίνει ότι απελευθερώνει θερμότητα. Αυτό μπορεί να γίνει αισθητό ως ελαφρά αύξηση της θερμοκρασίας στο μίγμα της αντίδρασης.
5. Σχηματισμός αλατιού :
Το οξικό κάλιο, το προϊόν της αντίδρασης, είναι ένα άλας. Τα άλατα είναι ιοντικές ενώσεις που αποτελούνται από θετικά φορτισμένα ιόντα (κατιόντα) και αρνητικά φορτισμένα ιόντα (Anions). Σε αυτή την περίπτωση, τα ιόντα καλίου (Κ+) δρουν ως κατιόντα και τα ιόντα οξικού (ch₃coo-) δρουν ως ανιόντα.
Συνοπτικά, όταν το οξικό οξύ αντιδρά με υδροξείδιο του καλίου, μπορούν να γίνουν οι ακόλουθες παρατηρήσεις:ο σχηματισμός οξικού καλίου, μια αντίδραση εξουδετέρωσης, η μεταβολή του ρΗ, η απελευθέρωση θερμότητας και ο σχηματισμός ενός αλατιού.