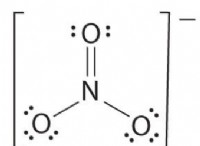
Πόσα μίλια νιτρικού ασβεστίου θα αντιδρούσε με 4,55 moles χρωμίου (III) θειικό για να παράγει νιτρικό χρώμιο;
Η ισορροπημένη χημική εξίσωση για την αντίδραση μεταξύ του νιτρικού ασβεστίου και του θειικού χρωμίου (III) είναι:
3CA (NO3) 2 + CR2 (SO4) 3 → 3CASO4 + 2CR (NO3) 3
Από την στοιχειομετρία της ισορροπημένης εξίσωσης, μπορούμε να δούμε ότι 3 γραμμομονείς νιτρικού ασβεστίου αντιδρούν με 1 mole του θειικού χρωμίου (III). Επομένως, θα απαιτούσε 4,55 moles του θειικού χρωμίου (iii):
(4.55 moles Cr2 (SO4) 3) × (3 moles Ca (NO3) 2/1 mole CR2 (SO4) 3) =13,65 moles Ca (NO3) 2
Τώρα, πρέπει να μετατρέψουμε τα μολυσμένα νιτρικά ασβέστιο σε μίλια. Η μοριακή μάζα νιτρικού ασβεστίου είναι περίπου 236 g/mol. Έτσι, 13,65 moles νιτρικού ασβεστίου είναι ισοδύναμα με:
(13,65 moles Ca (NO3) 2) × (236 g/mol) =3224 g Ca (NO3) 2
Υποθέτοντας πυκνότητα 2,5 g/cm3 για νιτρικό ασβέστιο, μπορούμε να υπολογίσουμε τον όγκο των 3224 g νιτρικού ασβεστίου:
Όγκος =μάζα/πυκνότητα =(3224 g)/(2,5 g/cm3) =1289 cm3
Τέλος, μπορούμε να μετατρέψουμε την ένταση σε μίλια πολλαπλασιάζοντας τον κατάλληλο συντελεστή μετατροπής:
1 μίλι =160934,4 cm
Επομένως, 1289 cm3 =(1289 cm³) × (1 μίλι / 160934.4 cm3) ≈ 0.008 μίλια
Έτσι, θα απαιτηθούν περίπου 0,008 μίλια νιτρικού ασβεστίου για να αντιδράσουν με 4,55 γραμμομονείς θειικού χρώματος (III).