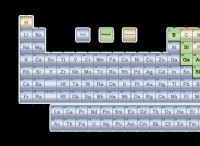
Το νάτριο και το χλώριο βρίσκονται στην ίδια περίοδο στον περιοδικό πίνακα εξηγούν τη διαφορά τους;
* Ατομική δομή: Καθώς μετακινείτε μια περίοδο από αριστερά προς τα δεξιά, αυξάνεται ο αριθμός των πρωτονίων στον πυρήνα. Αυτό το αυξημένο θετικό φορτίο προσελκύει τα αρνητικά φορτισμένα ηλεκτρόνια πιο έντονα, τραβώντας το σύννεφο ηλεκτρονίων πιο κοντά στον πυρήνα.
* νάτριο έναντι χλωρίου:
* νάτριο (NA): Έχει 11 πρωτόνια και 11 ηλεκτρόνια. Το εξώτατο ηλεκτρόνιο του βρίσκεται στην τροχιά 3S.
* χλώριο (CL): Έχει 17 πρωτόνια και 17 ηλεκτρόνια. Τα εξώτατα ηλεκτρόνια του βρίσκονται στα τροχιακά 3 και 3p.
* Επίδραση στο μέγεθος: Επειδή το χλώριο έχει μεγαλύτερο πυρηνικό φορτίο (περισσότερα πρωτόνια), τα ηλεκτρόνια του σχεδιάζονται πιο σφιχτά. Αυτό κάνει το χλώριο μικρότερο από το νάτριο, παρόλο που και τα δύο στοιχεία έχουν τα εξώτατα ηλεκτρόνια τους στο ίδιο επίπεδο ενέργειας (3ο επίπεδο ενέργειας).
Συνοπτικά:
* νάτριο (NA): Μεγαλύτερο ατομικό μέγεθος λόγω της ασθενέστερης έλξης μεταξύ του πυρήνα και του εξωτερικού ηλεκτρονίου.
* χλώριο (CL): Μικρότερο ατομικό μέγεθος λόγω της ισχυρότερης έλξης μεταξύ του πυρήνα και των εξωτερικών ηλεκτρονίων.
Επιτρέψτε μου να ξέρω αν έχετε άλλες ερωτήσεις!