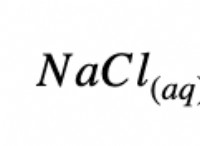Τι είναι το υδατικό νιτρικό ασήμι και το βρωμιούχο κάλιο συνδυάζονται για να σχηματίσουν ένα ίζημα;
Εδώ είναι η ισορροπημένη χημική εξίσωση για την αντίδραση:
agno₃ (aq) + kbr (aq) → AGBR (s) + kno₃ (aq)
Επεξήγηση:
* Νιτρικό άργυρο (agno₃) και βρωμιούχο κάλιο (KBR) είναι και οι δύο διαλυτές ιοντικές ενώσεις, που σημαίνει ότι διαλύονται στο νερό και υπάρχουν ως ιόντα.
* Όταν αναμιγνύεται, τα ασημένια ιόντα (Ag⁺) από νιτρικό άργυρο αντιδρούν με τα ιόντα βρωμιδίου (Br⁻) από βρωμιούχο κάλιο.
* Αυτή η αντίδραση σχηματίζει ασημένιο βρωμίδιο (AGBR) , που είναι αδιάλυτο στο νερό και επομένως κατακρημνίζεται ως στερεό.
* Τα υπόλοιπα ιόντα, κάλιο (k⁺) και νιτρικά (no₃⁻), παραμένουν σε διάλυμα ως υδατικό νιτρικό κάλιο (kno₃) .
Βασικά σημεία:
* Το ίζημα, ασημένιο βρωμίδιο , είναι ένα ανοιχτό κίτρινο στερεό.
* Αυτή η αντίδραση είναι ένα κλασικό παράδειγμα μιας αντίδρασης βροχόπτωσης , όπου δύο διαλυτές ιοντικές ενώσεις αντιδρούν για να σχηματίσουν ένα αδιάλυτο προϊόν.
* Η αντίδραση οδηγείται από το σχηματισμό του αδιάλυτου ασημένιου βρωμιούχου.