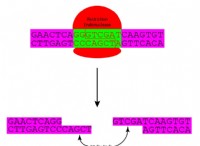
Ένας δεσμός σχηματίζεται μέσω μιας αδύναμης ηλεκτρικής έλξης μεταξύ του ατόμου υδρογόνου δεσμευμένο σε ένα ηλεκτρονατιενιετόμ, όπως το οξυγόνο και το άζωτο, ένα άλλο ηλεκτροαρνητικό άτομο;
Ακολουθεί μια κατανομή των βασικών σημείων:
* Αδύναμη ηλεκτρική έλξη: Οι δεσμοί υδρογόνου είναι πράγματι αδύναμοι σε σύγκριση με τους ομοιοπολικούς ή ιοντικούς δεσμούς. Προκύπτουν από την άνιση κατανομή των ηλεκτρονίων σε έναν ομοιοπολικό δεσμό μεταξύ του υδρογόνου και ενός εξαιρετικά ηλεκτροαρνητικού ατόμου όπως το οξυγόνο ή το άζωτο.
* Ηλεκτροργατιστικότητα: Το ηλεκτροαρνητικό άτομο (οξυγόνο ή άζωτο) τραβά τα κοινά ηλεκτρόνια πιο κοντά στον εαυτό του, δημιουργώντας ένα μερικό αρνητικό φορτίο (δ-) στο ηλεκτροαρνητικό άτομο και ένα μερικό θετικό φορτίο (δ+) στο άτομο υδρογόνου.
* έλξη: Αυτή η διαφορά στο φορτίο δημιουργεί μια ελκυστική δύναμη μεταξύ του μερικώς θετικού ατόμου υδρογόνου και του μοναχικού ζεύγους ηλεκτρονίων σε ένα κοντινό ηλεκτροαρνητικό άτομο (συχνά σε άλλο μόριο).
Σημασία των δεσμών υδρογόνου:
Οι δεσμοί υδρογόνου είναι απίστευτα σημαντικοί στη βιολογία και τη χημεία:
* νερό: Είναι υπεύθυνοι για τις μοναδικές ιδιότητες του νερού, όπως το υψηλό σημείο βρασμού και την ικανότητά του να διαλύουν πολλές ουσίες.
* πρωτεΐνες: Βοηθούν στη σταθεροποίηση των τρισδιάστατων δομών πρωτεϊνών, οι οποίες είναι ζωτικής σημασίας για τη λειτουργία τους.
* DNA: Συνεχίζουν τα δύο σκέλη του DNA, σχηματίζοντας τη διάσημη διπλή έλικα.
Επιτρέψτε μου να ξέρω αν θέλετε να εξερευνήσετε κάποιο από αυτά τα σημεία με περισσότερες λεπτομέρειες!