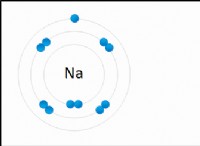
Όταν καίγεται το διάλυμα ψευδαργύρου που παρατηρείται το χρώμα της φλόγας;
* Λύσεις ψευδαργύρου: Τα διαλύματα ψευδαργύρου είναι συνήθως με τη μορφή αλάτων που διαλύονται σε νερό (όπως το θειικό ψευδάργυρο ή το χλωριούχο ψευδάργυρο). Η καύση μιας τέτοιας λύσης θα περιλαμβάνει κυρίως την καύση του νερού, όχι τον ίδιο τον ψευδάργυρο.
* Μέταλλο ψευδαργύρου: Για να παρατηρήσετε ένα χρώμα φλόγας, θα χρειαστεί να κάψετε στερεό μέταλλο ψευδαργύρου.
* Χρώμα φλόγας ψευδαργύρου: Όταν καίγεται μέταλλο ψευδαργύρου, παράγει μια φωτεινή μπλε-πράσινη φλόγα .
Εδώ είναι μια κατανομή της διαδικασίας:
1. Θερμότητα: Όταν θερμαίνετε το μέταλλο ψευδαργύρου, αντιδρά με οξυγόνο στον αέρα.
2. Οξείδωση: Αυτή η αντίδραση σχηματίζει οξείδιο ψευδαργύρου (ZnO).
3. Φλόγα: Η ενέργεια που απελευθερώνεται κατά τη διάρκεια αυτής της διαδικασίας οξείδωσης δημιουργεί τη χαρακτηριστική μπλε-πράσινη φλόγα.
Επιτρέψτε μου να ξέρω αν έχετε άλλες ερωτήσεις σχετικά με τον ψευδάργυρο ή τις φλόγες!