Γιατί λέμε ότι οι χημικές αντιδράσεις περιλαμβάνουν πάντα αλλαγές στην ενέργεια;
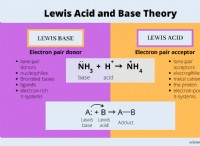
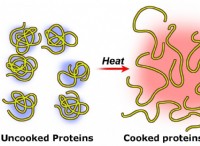
* Το σπάσιμο των δεσμών απαιτεί ενέργεια: Οι χημικοί δεσμοί αποθηκεύουν ενέργεια. Για να σπάσει ένας δεσμός, πρέπει να παρέχεται ενέργεια. Αυτή η ενέργεια παρέχεται συχνά ως θερμότητα, φως ή ηλεκτρική ενέργεια.
* Ο σχηματισμός δεσμών απελευθερώνει ενέργεια: Όταν σχηματίζονται νέα ομόλογα, η ενέργεια απελευθερώνεται. Αυτή η απελευθέρωση μπορεί να έχει τη μορφή θερμότητας, φωτός ή ακόμα και ήχου.
Η καθαρή αλλαγή ενέργειας:
Η συνολική ενεργειακή αλλαγή μιας χημικής αντίδρασης εξαρτάται από τη διαφορά μεταξύ της ενέργειας που απαιτείται για να σπάσει τους δεσμούς των αντιδραστηρίων και την ενέργεια που απελευθερώνεται όταν σχηματίζονται νέα δεσμοί στα προϊόντα.
* ενδοθερμικές αντιδράσεις: Εάν απαιτείται περισσότερη ενέργεια για να σπάσει τους δεσμούς από ό, τι απελευθερώνεται όταν σχηματίζονται νέοι δεσμοί, η αντίδραση απορροφά την ενέργεια από το περιβάλλον. Αυτή είναι μια ενδοθερμική αντίδραση.
* Εξοθερμικές αντιδράσεις: Εάν απελευθερωθεί περισσότερη ενέργεια όταν σχηματίζονται νέα ομόλογα από ό, τι απαιτείται για να σπάσει τους δεσμούς, η αντίδραση απελευθερώνει ενέργεια στο περιβάλλον. Αυτή είναι μια εξωθερμική αντίδραση.
Συμπερασματικά:
Κάθε χημική αντίδραση περιλαμβάνει το σπάσιμο και το σχηματισμό χημικών δεσμών και αυτή η διαδικασία οδηγεί αναπόφευκτα σε μια ενεργειακή αλλαγή, είτε απορροφώντας ενέργεια από το περιβάλλον είτε απελευθερώνοντας ενέργεια σε αυτά.