Εξηγήστε τι συμβαίνει όταν το διάλυμα υδροξειδίου του νατρίου προστίθεται στο υδροξείδιο του αμμωνίου;
NaOH (aq) + NH
Ακολουθεί μια ανάλυση του τι συμβαίνει:
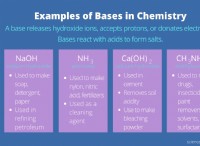
* Υδροξείδιο του νατρίου (NaOH) είναι μια ισχυρή βάση, που σημαίνει ότι διαχωρίζεται εντελώς σε διάλυμα για να σχηματίσει ιόντα νατρίου (Na
* Υδροξείδιο του αμμωνίου (NH <υπο -> OH) είναι μια αδύναμη βάση, που σημαίνει ότι μόνο εν μέρει διαχωρίζεται σε διάλυμα για να σχηματίσει ιόντα αμμωνίου (NH 4
* Τα ιόντα υδροξειδίου (oh
* Το αέριο αμμωνίας απελευθερώνεται ως φυσαλίδες , δημιουργώντας μια χαρακτηριστική έντονη οσμή.
Βασικές παρατηρήσεις:
* Παραγωγή αερίου αμμωνίας: Θα παρατηρήσετε τη διακριτική οσμή αμμωνίας, επιβεβαιώνοντας το σχηματισμό αερίου αμμωνίας.
* Η λύση γίνεται λιγότερο βασική: Η προσθήκη ΝΑΟΗ μειώνει τη συγκέντρωση υδροξειδίου του αμμωνίου, με αποτέλεσμα ένα λιγότερο βασικό διάλυμα.
Συνολικά, η αντίδραση έχει ως αποτέλεσμα το σχηματισμό των ιόντων αερίου αμμωνίας, νερού και νατρίου, καθιστώντας το διάλυμα λιγότερο βασικό.