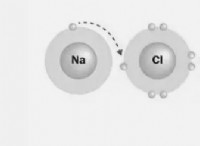
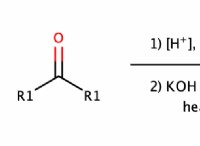
Τι προκαλεί τη διάσπαση των δεσμών σε χημικές αντιδράσεις;
* Bonds Store Energy: Οι χημικοί δεσμοί αντιπροσωπεύουν αποθηκευμένη ενέργεια. Οι ισχυρότεροι δεσμοί κατέχουν περισσότερη ενέργεια.
* Η είσοδος ενέργειας ξεπερνά την αντοχή του δεσμού: Όταν παρέχεται αρκετή ενέργεια, μπορεί να ξεπεράσει τις ελκυστικές δυνάμεις που συγκρατούν τα άτομα μαζί σε έναν δεσμό, προκαλώντας τη διάσπαση του δεσμού.
* Πηγές ενέργειας: Αυτή η εισροή ενέργειας μπορεί να προέρχεται από διάφορες πηγές:
* Θερμότητα: Η θέρμανση μιας ουσίας παρέχει κινητική ενέργεια στα μόρια, αυξάνοντας τη δονητική τους κίνηση και ενδεχομένως αποδυνάμωση δεσμών.
* φως: Ορισμένα μήκη κύματος του φωτός μπορούν να απορροφηθούν από μόρια, παρέχοντας ενέργεια για να σπάσουν τους δεσμούς (σκεφτείτε τη φωτοσύνθεση).
* Ηλεκτρική ενέργεια: Το ηλεκτρικό ρεύμα μπορεί να προκαλέσει τη ροή των ηλεκτρονίων, τα οποία μπορούν να διαταράξουν τα ομόλογα.
* Άλλες χημικές αντιδράσεις: Η ενέργεια που απελευθερώνεται από μία χημική αντίδραση μπορεί να χρησιμοποιηθεί για να σπάσει τους δεσμούς σε μια άλλη αντίδραση.
Βασικές έννοιες:
* Ενέργεια ενεργοποίησης: Η ελάχιστη ποσότητα ενέργειας που απαιτείται για να ξεκινήσει μια χημική αντίδραση. Είναι η ενέργεια που απαιτείται για να ξεπεραστεί η αρχική σταθερότητα των αντιδραστηρίων και να σπάσει τους δεσμούς.
* ενδοθερμικές και εξωθερμικές αντιδράσεις:
* ενδοθερμικές αντιδράσεις: Απαιτούν εισροή ενέργειας για να προχωρήσει. Το Breaking Bond απαιτεί περισσότερη ενέργεια από ό, τι απελευθερώνεται όταν η μορφή νέων ομολόγων.
* Εξοθερμικές αντιδράσεις: Απελευθερώστε ενέργεια στο περιβάλλον. Ο σχηματισμός νέων ομολόγων απελευθερώνει περισσότερη ενέργεια από ό, τι χρειάστηκε για να σπάσει τα αρχικά ομόλογα.
Συνοπτικά:
Οι χημικές αντιδράσεις περιλαμβάνουν το σπάσιμο και τον σχηματισμό των δεσμών. Το σπάσιμο των δεσμών απαιτεί μια εισροή ενέργειας για να ξεπεραστεί οι ελκυστικές δυνάμεις που συγκρατούν τα άτομα μαζί. Αυτή η ενέργεια μπορεί να παρέχεται από θερμότητα, φως, ηλεκτρικό ρεύμα ή άλλες χημικές αντιδράσεις.