Τα μεταλλικά στοιχεία τείνουν να σχηματίζουν κατιόντα και όχι ανιόντα;
* Ηλεκτροργατιστικότητα: Τα μεταλλικά στοιχεία έχουν σχετικά χαμηλή ηλεκτροαρνητικότητα. Αυτό σημαίνει ότι έχουν μια ασθενέστερη έλξη για τα ηλεκτρόνια σε σύγκριση με τα μη μέταλλα.
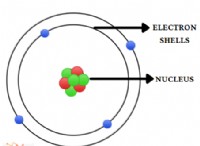
* Διαμόρφωση ηλεκτρονίων: Τα μέταλλα έχουν συνήθως μερικά ηλεκτρόνια σθένους (ηλεκτρόνια στο εξώτατο κέλυφος). Τείνουν να χάσουν αυτά τα ηλεκτρόνια σθένους για να επιτύχουν μια σταθερή, γεμάτη διαμόρφωση ηλεκτρονίων.
* ενέργεια ιονισμού: Τα μέταλλα έχουν σχετικά χαμηλές ενέργειες ιονισμού, πράγμα που σημαίνει ότι είναι σχετικά εύκολο να χάσουν ηλεκτρόνια.
Παράδειγμα: Το νάτριο (Na) έχει ένα ηλεκτρόνιο σθένους. Χάνει εύκολα αυτό το ηλεκτρόνιο για να γίνει κατιόν νατρίου (Na+), το οποίο έχει την ίδια διαμόρφωση ηλεκτρονίων με το NEON NEON NEON (NE).
Εξαιρέσεις:
Ενώ τα περισσότερα μέταλλα σχηματίζουν κατιόντα, υπάρχουν κάποιες εξαιρέσεις. Μερικά μέταλλα, όπως ο χρυσός (AU) και η πλατίνα (PT), μπορούν να σχηματίσουν ανιόντα υπό πολύ συγκεκριμένες συνθήκες. Αυτό συμβαίνει συνήθως όταν συνδέονται με πολύ ηλεκτροαρνητικά στοιχεία όπως το φθόριο.
Συνοπτικά: Η τάση των μετάλλων να χάσουν ηλεκτρόνια και σχηματισμό κατιόντων είναι ένα θεμελιώδες χαρακτηριστικό της χημικής τους συμπεριφοράς.