Γιατί η φαινυλαλανίνη είναι μη πολική;
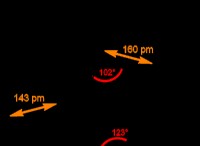
1. πλευρική αλυσίδα υδρογονανθράκων: Η φαινυλαλανίνη έχει δακτύλιο βενζολίου (C6H6) που συνδέεται με την πλευρική του αλυσίδα. Οι δακτύλιοι βενζολίου αποτελούνται εξ ολοκλήρου από άτομα άνθρακα και υδρογόνου, τα οποία είναι μη πολικά. Αυτή η μεγάλη πλευρική αλυσίδα υδρογονανθράκων συμβάλλει σημαντικά στη μη πολική φύση του αμινοξέος.
2. Έλλειψη πολικών ομάδων: Η φαινυλαλανίνη δεν διαθέτει πολικές λειτουργικές ομάδες, όπως οι ομάδες υδροξυλίου (-ΟΗ), αμινο (-ΝΗ2) ή καρβοξυλίου (-COOH), οι οποίες θα εισήγαγαν πολικότητα.
3. υδρόφοβες αλληλεπιδράσεις: Η μη πολική φύση της φαινυλαλανίνης της επιτρέπει να αλληλεπιδράσει ευνοϊκά με άλλα μη πολωτικά μόρια μέσω υδρόφοβων αλληλεπιδράσεων. Αυτές οι αλληλεπιδράσεις είναι ζωτικής σημασίας για την αναδίπλωση των πρωτεϊνών και τον σχηματισμό σταθερών πρωτεϊνικών δομών.
4. Διαλυτότητα: Η φαινυλαλανίνη είναι κακώς διαλυτή στο νερό, υποδεικνύοντας περαιτέρω τη μη πολική φύση της. Το νερό είναι ένας πολικός διαλύτης και τα μη πολικά μόρια τείνουν να είναι αδιάλυτα σε αυτό.
Συνοπτικά, η μεγάλη πλευρική αλυσίδα υδρογονανθράκων της φαινυλαλανίνης, η απουσία πολικών λειτουργικών ομάδων και οι υδρόφοβες αλληλεπιδράσεις της συμβάλλουν στην ταξινόμησή της ως μη πολικού αμινοξέος.