Ποια είναι η πιο σταθερή εξωτερική τροχιακή διάταξη των ηλεκτρονίων μετά από χημική αντίδραση;
Εδώ είναι γιατί αυτή η ρύθμιση είναι η πιο σταθερή:
* Συμπληρωματικό κέλυφος σθένους: Τα άτομα με πλήρες εξωτερικό κέλυφος έχουν χαμηλότερη κατάσταση ενέργειας και είναι πιο σταθερά. Αυτό οφείλεται στο γεγονός ότι τα ηλεκτρόνια συνδέονται στενά με τον πυρήνα, ελαχιστοποιώντας την πιθανή ενέργεια τους.
* Μειωμένη αντιδραστικότητα: Ένα γεμάτο κέλυφος σθένους κάνει το άτομο λιγότερο αντιδραστικό, καθώς δεν έχει έντονη τάση να κερδίζει ή να χάνει ηλεκτρόνια για να σχηματίσει χημικούς δεσμούς.
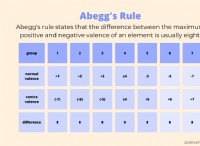
Εξαιρέσεις από τον κανόνα οκτάδων:
* υδρογόνο και ήλιο: Αυτά τα στοιχεία χρειάζονται μόνο δύο ηλεκτρόνια για να επιτύχουν μια σταθερή διαμόρφωση.
* Στοιχεία στην τρίτη περίοδο και πέρα: Λόγω της διαθεσιμότητας D τροχιακών, ορισμένα στοιχεία μπορούν να φιλοξενήσουν περισσότερα από οκτώ ηλεκτρόνια στο κέλυφος σθένους τους. Για παράδειγμα, ο φωσφόρος μπορεί να έχει 10 ηλεκτρόνια στο εξωτερικό του κέλυφος.
Συνοπτικά:
Η πιο σταθερή εξωτερική τροχιακή διάταξη των ηλεκτρονίων μετά από μια χημική αντίδραση είναι αυτή που ικανοποιεί τον κανόνα οκτάδων (με εξαιρέσεις), επιτυγχάνοντας ένα πλήρες κέλυφος σθένους και ελάχιστη αντιδραστικότητα.