Εισαγωγή στην τιμή pH των τροφίμων (&αντιδράσεις οξέος/βάσης)
Ο χυμός κόκκινου λάχανου αλλάζει χρώμα όταν προσθέτετε ένα squirt χυμό λάιμ ή μια κουταλιά μαγειρική σόδα. Το μπέικιν πάουντερ κάνει το κέικ σας να φουσκώσει όμορφα στο φούρνο. Μπορείτε να «μαγειρέψετε» ψάρια προσθέτοντας χυμό λεμονιού και λάιμ, αυτό κάνει ένα ceviche.
Τι κοινό έχουν όλα αυτά τα παραδείγματα;
Είναι όλα παραδείγματα αντιδράσεων οξέος/βάσης. Αυτοί οι τύποι αντιδράσεων είναι μόνο μία από τις πολλές χημικές αντιδράσεις που συμβαίνουν στα τρόφιμα (μια άλλη θα ήταν το ρόφημα των μπανανών). Οι αντιδράσεις οξέος/βάσης έχουν όλες πολλά κοινά, παρόλο που η επίδρασή τους (αλλαγή χρώματος, ζυμωτό κέικ ή «μαγειρεμένο» ψάρι) μπορεί να φαίνεται πολύ διαφορετικό. Σε αυτήν την ανάρτηση θα συζητήσουμε την υποκείμενη επιστήμη αυτών των τύπων αντιδράσεων.
Πότε ένα τρόφιμο είναι όξινο;
Τα όξινα τρόφιμα είναι αρκετά κοινά. Ο χυμός λεμονιού και λάιμ, το ξύδι, το γιαούρτι και το βουτυρόγαλα είναι όλα όξινα τρόφιμα. Αν πιείτε κάποιο από αυτά, θα γευτείτε την οξύτητα.
Το αντίθετο από ένα όξινο φαγητό (ή ποτό) είναι αυτό που είναι αλκαλικό. Ένα καλό παράδειγμα αυτού είναι η μαγειρική σόδα. Ένα τρόφιμο που δεν είναι ούτε όξινο ούτε αλκαλικό ονομάζεται ουδέτερο.
Το αν κάτι είναι όξινο ή αλκαλικό ή όχι είναι πολύ καλά καθορισμένο από τους χημικούς. Για να προσδιορίσετε τι είναι τρόφιμο, χρησιμοποιείτε την κλίμακα pH. Αυτή η κλίμακα κυμαίνεται από 0-14. Κάθε τρόφιμο που έχει τιμή pH 7 είναι ουδέτερο. Τα τρόφιμα με pH χαμηλότερο από 7 είναι όξινα, αυτά με pH υψηλότερο από 7 είναι αλκαλικά.
Όσο πιο μακριά από αυτή την ουδέτερη τιμή του 7 τόσο πιο όξινο (ή αλκαλικό) είναι ένα τρόφιμο. Για παράδειγμα, ο χυμός λεμονιού έχει τιμή pH 2-3, ενώ του γιαουρτιού είναι περίπου 4-4,5. Ως εκ τούτου, ο χυμός λεμονιού είναι πιο όξινος από το γιαούρτι.
Προσδιορισμός της τιμής pH
Μπορείτε να μετρήσετε την τιμή pH ενός τροφίμου χρησιμοποιώντας ένα pH-meter ή μια ειδική ταινία μέτρησης pH. Εάν χρησιμοποιείτε pH-μετρητή, μπορείτε να πάρετε μια συγκεκριμένη τιμή για το προϊόν που μετράτε, π.χ. 2.3. Ωστόσο, δεδομένου ότι τα τρόφιμα είναι εκ φύσεως αρκετά διαφορετικά, μπορεί να υπάρχουν πολλές διαφορές μεταξύ παρόμοιων τροφίμων. Ένα λεμόνι μπορεί να έχει τιμή pH 2,1 ενώ ένα άλλο μπορεί να είναι 2,4. Αυτός είναι ο λόγος που βλέπετε συχνά σειρές για συγκεκριμένα τρόφιμα.
Παραδείγματα τιμών pH στα τρόφιμα
Τα τρόφιμα έχουν ένα ευρύ φάσμα τιμών pH, αν και τα περισσότερα από αυτά είναι είτε γύρω στην τιμή 7 (άρα ουδέτερη) είτε χαμηλότερα από επτά. Δεδομένου ότι τα προϊόντα διατροφής, ειδικά τα φρέσκα τρόφιμα, όπως τα φρούτα και τα λαχανικά και το κρέας, δεν είναι πολύ σταθερά στις ιδιότητές τους, η ακριβής τιμή pH θα διαφέρει ανά μεμονωμένο προϊόν. Πολλοί παράγοντες επηρεάζουν την τιμή του pH, μεταξύ άλλων η ωρίμανση του προϊόντος. Η παρακάτω λίστα παρέχει ορισμένες γενικές οδηγίες (πηγή).
- Μήλα:3,3 – 4,0
- Αβοκάντο:6,2 – 6,6
- Μελιτζάνες:4,5 – 5,3
- Μαρμελάδα φρούτων:3,5 – 4,5
- Μέλι:3,9
- Ξίδι:2,0 – 3,4
Σε τι χρησιμεύει η τιμή pH στην επιστήμη των τροφίμων;
Η τιμή του pH επηρεάζει τη γεύση του φαγητού σας, αλλά μπορεί επίσης να είναι πολύ σημαντική για τη διάρκεια ζωής του φαγητού σας, πόσο καιρό παραμένει ασφαλές. Το φαγητό μπορεί να χαλάσει και να χαλάσει εξαιτίας της ανάπτυξης ανεπιθύμητων μικροοργανισμών. Ωστόσο, πολλοί μικροοργανισμοί δεν αναπτύσσονται πια όταν η τιμή του pH έχει πέσει κάτω από μια συγκεκριμένη τιμή. Ως εκ τούτου, η επαρκής μείωση της τιμής του pH θα διατηρήσει τα τρόφιμα ασφαλή περισσότερο.
Εκτός από τη διάρκεια ζωής, η τιμή pH μπορεί να χρησιμοποιηθεί για την παρακολούθηση των διαδικασιών τροφίμων. Για παράδειγμα, η παρασκευή γιαουρτιού συνίσταται κυρίως στη μείωση της τιμής του pH του γάλακτος. Λόγω της χαμηλότερης τιμής pH, το γάλα θα πήξει. Οι κατασκευαστές θα γνωρίζουν σε ποια τιμή pH ολοκληρώνεται η διαδικασία. Με αυτόν τον τρόπο, μετρώντας αυτήν την τιμή μπορούν να παρακολουθούν τη διαδικασία, χωρίς να χρειάζεται να κοιτάξουν ή να δοκιμάσουν το προϊόν.

Τι είναι η τιμή pH
Τι είναι λοιπόν αυτό που κάνει αυτές τις τροφές αλκαλικές ή όξινες; Ενώ η ζάχαρη κάνει κάτι γλυκό και το αλάτι κάτι αλμυρό, τα πρωτόνια κάνουν κάτι όξινο.
Πρωτόνια
Τα πρωτόνια είναι μεμονωμένα άτομα υδρογόνου (Η) που χάνουν το ηλεκτρόνιό τους. Ως αποτέλεσμα, είναι θετικά φορτισμένα. Οι χημικοί καταγράφουν τα πρωτόνια ως:H.
Τα πρωτόνια παίζουν ρόλο σε πολλές αντιδράσεις στο ανθρώπινο σώμα και στους περισσότερους ζωντανούς οργανισμούς. Από πού προέρχονται λοιπόν;
Ένας τρόπος είναι μέσω μορίων που είναι φυσικά όξινα (π.χ. κιτρικό οξύ). Αυτοί απομακρύνουν ένα από τα πρωτόνια τους πολύ εύκολα. Όταν το κάνουν, η συγκέντρωση των πρωτονίων αυξάνεται. Εάν η συγκέντρωση των πρωτονίων αυξηθεί, η τιμή pH του τροφίμου μειώνεται. Περισσότερα πρωτόνια, σημαίνει περισσότερη οξύτητα. Αυτή η σχέση μπορεί να εκφραστεί με τον ακόλουθο τύπο:
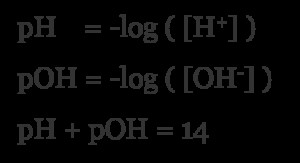
Όπως μπορείτε να δείτε σε αυτούς τους τύπους, υπάρχει μια ισορροπία μεταξύ πρωτονίων (Η) και ιόντων υδροξειδίου (ΟΗ). Είναι το ένα το αντίστροφο του άλλου. Περισσότερα πρωτόνια σημαίνει χαμηλότερη τιμή pH, ενώ περισσότερα ιόντα υδροξειδίου έχουν ως αποτέλεσμα υψηλότερη τιμή pH (ή χαμηλότερη τιμή pOH). Συνηθέστερα θα βρείτε μόνο τιμές pH, η τιμή pOH χρησιμοποιείται ελάχιστα στην πράξη. Αυτή η σχέση είναι ο πυρήνας των αντιδράσεων οξέος/βάσης και έχει την προέλευσή της στο μόριο του νερού.
Νερό και οξύτητα
Το ίδιο το νερό είναι ουδέτερο αλλά μπορεί να διασπαστεί τόσο σε πρωτόνιο όσο και σε ιόν υδροξειδίου.

Αντί να δούμε το μοναδικό πρωτόνιο, ένα ιόν υδρονίου (H3 Ο) σχηματίζεται. Με την παρουσία νερού αυτό θα συμβεί και γι' αυτό σε πολλές περιπτώσεις μπορείτε να τα χρησιμοποιήσετε εναλλάξιμα. (Εάν δεν είστε εξοικειωμένοι με την καταγραφή των χημικών αντιδράσεων, διαβάστε πρώτα τα βασικά στοιχεία της χημικής αντίδρασης.)
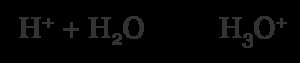
Σε ένα ουδέτερο περιβάλλον, υπάρχει ίση ποσότητα πρωτονίων (Η) και ιόντων υδροξειδίου (ΟΗ). Μόνο αν η τροφή είναι όξινη είναι αλκαλική, αυτή η ισορροπία είναι εκτός λειτουργίας. Τα όξινα μόρια ή τα αλκαλικά μόρια μπορούν είτε να αυξήσουν την περιεκτικότητα σε πρωτόνια είτε σε υδροξείδιο.
Όταν ένα οξύ (ΑΗ στο παρακάτω παράδειγμα) υπάρχει στο νερό, μειώνει την τιμή του pH απελευθερώνοντας ένα πρωτόνιο:

Από την άλλη πλευρά, όταν υπάρχει μια αλκαλική ουσία, θα σχηματίσει ένα ιόν υδροξειδίου, με αποτέλεσμα η υγρασία να είναι πιο αλκαλική.

Αντιδράσεις οξέος/βάσης
Αυτή η τιμή pH είναι ένας ισχυρός δείκτης των τύπων χημικών αντιδράσεων που μπορούν να συμβούν. Διαφορετικοί τύποι αντιδράσεων μπορούν να συμβούν σε όξινα περιβάλλοντα σε αντίθεση με τα αλκαλικά.
Όλες οι αντιδράσεις οξέος/βάσης έχουν κοινό ότι ανταλλάσσονται πρωτόνια. Ένα οξύ θα δώσει ένα πρωτόνιο (αυξάνοντας τη συγκέντρωση των πρωτονίων, μειώνοντας έτσι το pH). Μια αλκαλική ουσία από την άλλη πλευρά θα τείνει να πάρει ένα πρωτόνιο.
Ας ρίξουμε μια ματιά ξανά στις αντιδράσεις που είδαμε προηγουμένως. Ρίξτε μια ματιά στο πώς ανταλλάσσονται αυτά τα πρωτόνια.


Αντιδράσεις ισορροπίας
Ένα πράγμα που μπορεί να παρατηρήσετε σε αυτές τις αντιδράσεις είναι τα διπλά βέλη και στα δύο. Αυτά τα διπλά βέλη δείχνουν ότι πρόκειται για αντίδραση ισορροπίας. Με άλλα λόγια, η αντίδραση μπορεί να συμβεί από αριστερά προς τα δεξιά και από δεξιά προς τα αριστερά. Αυτό δεν σημαίνει ότι εμφανίζεται στον ίδιο βαθμό και στις δύο κατευθύνσεις.
Τα πολύ ισχυρά οξέα θα δώσουν (σχεδόν) όλα τα πρωτόνια τους. Αυτά ονομάζονται, κατάλληλα, ισχυρά οξέα. Στις περισσότερες περιπτώσεις όμως μόνο ένα ορισμένο ποσοστό των οξέων θα δώσει τα πρωτόνια τους. Αυτά είναι αδύναμα οξέα. Το ίδιο ισχύει και για τα αλκαλικά αντίστοιχα, τις βάσεις.
Πόσα από το οξύ θα δώσει το πρωτόνιό του μπορεί να εκφραστεί χρησιμοποιώντας μια σταθερά ισορροπίας. Για την εξίσωση οξέος (AH) που φαίνεται παραπάνω, μοιάζει με:
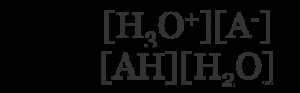
Το [ ] δείχνει συγκέντρωση. Δεδομένου ότι η συγκέντρωση του νερού είναι ουσιαστικά σταθερή, αυτό συχνά μένει έξω από την εξίσωση. Ένα οξύ που αποδίδει σχεδόν όλα τα πρωτόνια του θα έχει πολύ χαμηλή συγκέντρωση ΑΗ και υψηλή συγκέντρωση Α. Ως αποτέλεσμα, το Ka -Η τιμή θα είναι μεγάλη. Όσο μεγαλύτερο είναι το Ka -τιμή, τόσο ισχυρότερο είναι το οξύ.
Είναι σημαντικό να γνωρίζουμε ότι αυτή η σταθερά ισορροπίας αλλάζει με τη θερμοκρασία. Έτσι, ένα οξύ μπορεί να απελευθερώσει πρωτόνια περισσότερο ή λιγότερο εύκολα σε διαφορετικές θερμοκρασίες.
Για μια αλκαλική ουσία η εξίσωση ισορροπίας είναι πολύ παρόμοια:

Εφαρμογή αντιδράσεων οξέος/βάσης
Στην πράξη δεν θα συζητήσετε το Ka και Kb αξίες συχνά. Ωστόσο, θα δείτε τα αποτελέσματά τους παντού γύρω σας. Η μαγειρική σόδα για παράδειγμα είναι ένα παράδειγμα αλκαλικού συστατικού τροφίμων. Η σύγκριση αυτών των χημικών αντιδράσεων με αυτούς τους βασικούς τύπους θα δείξει πολλές ομοιότητες.
Το ίδιο ισχύει και για το κόκκινο λάχανο. Το χρώμα του κόκκινου λάχανου αλλάζει με την τιμή pH του υγρού που το περιβάλλει. Αυτό προκαλείται από αντιδράσεις οξέος/βάσης με τα μόρια που δίνουν το χρώμα του στο κόκκινο λάχανο!
Φυσικά, το οξύ δεν αφορά μόνο τις χημικές αντιδράσεις. Είναι επίσης πολλά για τη γεύση και την ισορροπία ενός πιάτου. Ορισμένα πιάτα χρειάζονται απλώς λίγο οξύ (π.χ. χυμός λεμονιού) για να λειτουργήσουν καλά. Η Samin Nosrat κάνει εξαιρετική δουλειά εξηγώντας αυτή την πλευρά του οξέος στο βιβλίο της αλάτι, λίπος, οξύ, θερμότητα.
Αναφορές
Πανεπιστήμιο Clemson, τιμές pH των κοινών τροφίμων και συστατικών, σύνδεσμος; πηγή για τις τιμές pH των τροφίμων που αναφέρονται σε αυτό το άρθρο




