Υπολογισμοί Πυκνότητας – Εργασμένο Παράδειγμα Πρόβλημα

Η πυκνότητα είναι η μέτρηση της ποσότητας μάζας ανά μονάδα όγκου. Οι υπολογισμοί της πυκνότητας γίνονται χρησιμοποιώντας τον τύπο:
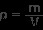
όπου
ρ =πυκνότητα
m =μάζα
V =τόμος
Παράδειγμα προβλημάτων:
1. Υπολογίστε την πυκνότητα σε g/mL 30 mL διαλύματος που ζυγίζει 120 γραμμάρια.
2. Υπολογίστε την πυκνότητα σε g/mL 0,4 L διαλύματος βάρους 150 γραμμαρίων.
3. Υπολογίστε την πυκνότητα σε g/mL 3000 mL διαλύματος βάρους 6 kg.
Παράδειγμα 1
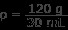
πυκνότητα =4 g/mL
Παράδειγμα 2
Θέλουμε να ξέρουμε την πυκνότητα σε g/mL, αλλά ο όγκος μας είναι σε λίτρα. Πρώτα, μετατρέψτε τον όγκο σε mL.
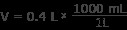
V=400 mL
Τώρα μπορούμε να υπολογίσουμε την πυκνότητα
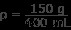
ρ =0,375 g/mL
Παράδειγμα 3
Και πάλι θέλουμε g/mL, και η μάζα μας είναι σε kg. Μετατρέψτε τη μάζα σε γραμμάρια.
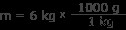
m =6000 γραμμάρια
Υπολογίστε την πυκνότητα
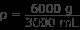
ρ =2 g/mL




