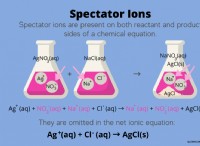
Τι είναι το pKa;
Βασικές έννοιες
Σε αυτό το σεμινάριο, θα μάθετε για το pKa και τις σχέσεις του με το Ka και το pH καθώς και τον τρόπο υπολογισμού του pKa από το Ka και το pH.
Θέματα που καλύπτονται σε άλλα άρθρα
- Χημεία οξέος-βάσης
- Ισχυρά οξέα και βάσεις
- Τύποι χημικών αντιδράσεων
- Ιδιότητες οξέων και βάσεων
Λεξιλόγιο
Bronsted Acid – κάθε είδος ικανό να δώσει ένα πρωτόνιο (H) σε άλλο μόριο.
Τι είναι το pKa;
Με απλά λόγια, το pKa είναι ένας αριθμός που δείχνει πόσο αδύναμο ή δυνατό είναι ένα οξύ. Ένα ισχυρό οξύ θα έχει pKa μικρότερο από μηδέν. Πιο συγκεκριμένα – το pKa είναι η αρνητική λογαριθμική βάση δέκα της τιμής Ka (σταθερά διάστασης οξέος). Μετρά την ισχύ ενός οξέος - πόσο σφιχτά συγκρατείται ένα πρωτόνιο από ένα οξύ Bronsted. Όσο χαμηλότερη είναι η τιμή του pKa, τόσο ισχυρότερο είναι το οξύ και τόσο μεγαλύτερη είναι η ικανότητά του να δίνει τα πρωτόνια του.
pKa και Ka
Το Ka υποδηλώνει τη σταθερά διάστασης οξέος. Μετρά πόσο πλήρως διασπάται ένα οξύ σε ένα υδατικό διάλυμα. Όσο μεγαλύτερη είναι η τιμή του Ka, τόσο ισχυρότερο είναι το οξύ καθώς το οξύ διασπάται σε μεγάλο βαθμό στα ιόντα του.
Ka έως pKa
Η σχέση μεταξύ pKa και Ka περιγράφεται από την ακόλουθη εξίσωση:
pKa =-log[Ka]
pKa σε Ka
Αντίστροφα, το Ka είναι μετρήσιμο όταν δίνεται pKa:
Ka =10
pKa και pH
Το pH είναι ένα μέτρο της συγκέντρωσης των ιόντων υδρογόνου σε ένα υδατικό διάλυμα. Όσο χαμηλότερη είναι η τιμή του pH, τόσο μεγαλύτερη είναι η συγκέντρωση ιόντων υδρογόνου στο διάλυμα. Επομένως, τόσο ισχυρότερο είναι το οξύ.
Το pKa και το pH σχετίζονται καθώς το pKa βοηθά στην πρόβλεψη του τι θα κάνει ένα μόριο σε ένα συγκεκριμένο pH. Ουσιαστικά, το pKa αποκαλύπτει ποιο πρέπει να είναι το pH για να μπορέσει ένα χημικό είδος να δωρίσει ή να δεχθεί ένα πρωτόνιο.
Η σχέση μεταξύ pKa και pH περιγράφεται από την εξίσωση Henderson-Hasselbalch:
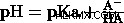
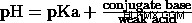
pKa ορισμένων αδύναμων και ισχυρών οξέων:
Υδροκυανικό οξύ pKa =9,21 (HCN, ασθενές οξύ):
Οξεικό οξύ pKa =4,75 (ασθενές οξύ)
Υδροφθορικό οξύ pKa =3,14 (HF, ασθενές οξύ)
Υδροχλωρικό οξύ pKa =-8 (HCl, ισχυρό οξύ):
Θειικό οξύ pKa ~ 3 (ισχυρό οξύ)
Μερικά περισσότερα pKa είναι εδώ.
Το αγαπημένο μας πείραμα χημείας
Χωρίς οξέα, με βάση ή pKA σε αυτό το βίντεο, απλά μια πολύ ωραία χημεία!