Διαφορά μεταξύ της θεωρίας του δεσμού σθένους και της θεωρίας των μοριακών τροχιακών
Κύρια διαφορά – Θεωρία δεσμού σθένους έναντι μοριακής τροχιακής θεωρίας
Ένα άτομο αποτελείται από τροχιακά όπου βρίσκονται τα ηλεκτρόνια. Αυτά τα ατομικά τροχιακά μπορούν να βρεθούν σε διαφορετικά σχήματα και σε διαφορετικά επίπεδα ενέργειας. Όταν ένα άτομο βρίσκεται σε ένα μόριο σε συνδυασμό με άλλα άτομα, αυτά τα τροχιακά είναι διατεταγμένα με διαφορετικό τρόπο. Η διάταξη αυτών των τροχιακών θα καθορίσει τον χημικό δεσμό και το σχήμα ή τη γεωμετρία του μορίου. Για να εξηγήσουμε τη διάταξη αυτών των τροχιακών, μπορούμε να χρησιμοποιήσουμε είτε τη θεωρία του δεσμού σθένους είτε τη θεωρία των μοριακών τροχιακών. Η κύρια διαφορά μεταξύ της θεωρίας του δεσμού σθένους και της θεωρίας των μοριακών τροχιακών είναι ότι η θεωρία του δεσμού σθένους εξηγεί τον υβριδισμό των τροχιακών ενώ η θεωρία των μοριακών τροχιακών δεν δίνει λεπτομέρειες σχετικά με τον υβριδισμό των τροχιακών.
Βασικές περιοχές που καλύπτονται
1. Τι είναι η θεωρία του δεσμού σθένους
– Ορισμός, Θεωρία, Παραδείγματα
2. Τι είναι η Μοριακή Τροχιακή Θεωρία
– Ορισμός, Θεωρία, Παραδείγματα
3. Ποια είναι η διαφορά μεταξύ της θεωρίας του δεσμού σθένους και της θεωρίας μοριακών τροχιακών
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Αντισυνδεδεμένα μοριακά τροχιακά, δεσμευτικά μοριακά τροχιακά, υβριδισμός, υβριδικά τροχιακά, μοριακή τροχιακή θεωρία, δεσμός Pi, δεσμός σίγμα, sp Orbital, spOrbital, spOrbital, spdOrbital, Θεωρία δεσμού σθένους 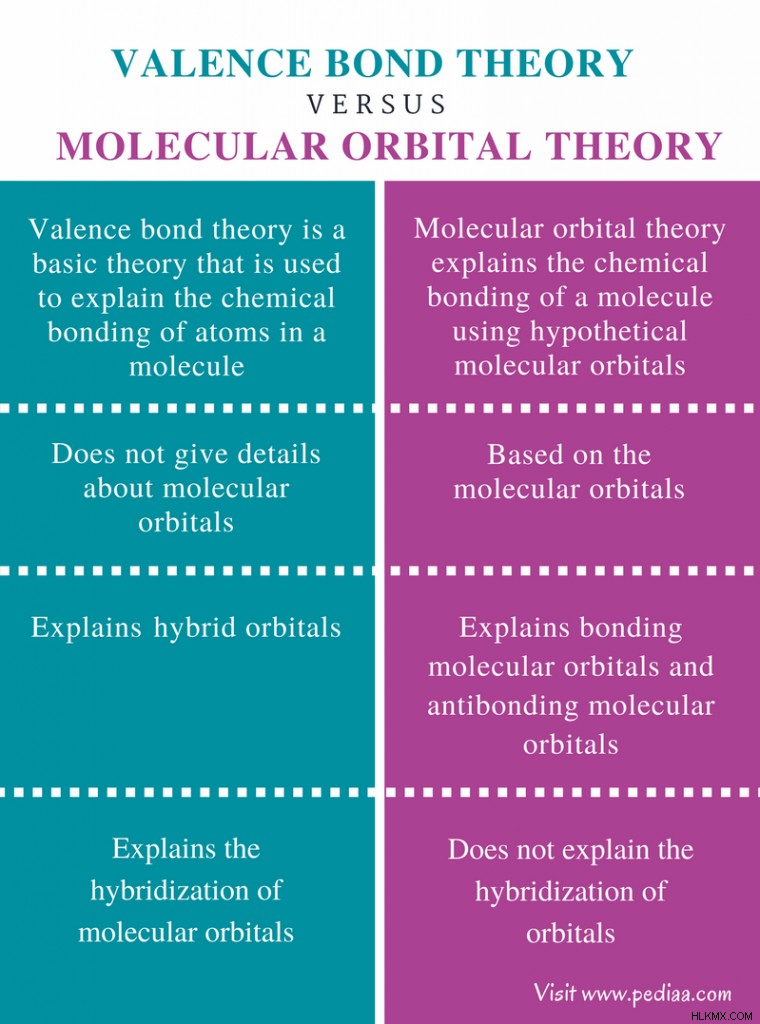
Τι είναι η θεωρία δεσμού σθένους
Η θεωρία του δεσμού σθένους είναι μια βασική θεωρία που χρησιμοποιείται για να εξηγήσει τους χημικούς δεσμούς των ατόμων σε ένα μόριο. Η θεωρία του δεσμού σθένους εξηγεί τη σύζευξη ηλεκτρονίων μέσω της επικάλυψης των τροχιακών. Τα ατομικά τροχιακά βρίσκονται κυρίως ως τροχιακά s, τροχιακά p και d τροχιακά. Σύμφωνα με τη θεωρία του δεσμού σθένους, η επικάλυψη δύο τροχιακών s ή η αλληλοεπικάλυψη τροχιακών p θα σχηματίσει έναν δεσμό σίγμα. Η επικάλυψη δύο παράλληλων τροχιακών p θα σχηματίσει έναν δεσμό pi. Επομένως, ένας απλός δεσμός θα περιέχει μόνο έναν δεσμό σίγμα ενώ ένας διπλός δεσμός θα περιέχει έναν δεσμό σίγμα και έναν δεσμό pi. Ένας τριπλός δεσμός μπορεί να περιέχει έναν δεσμό σίγμα μαζί με δύο δεσμούς pi.
Απλά μόρια όπως το H2 σχηματίζουν έναν δεσμό σίγμα απλώς με την επικάλυψη των τροχιακών αφού τα άτομα υδρογόνου (Η) αποτελούνται μόνο από τροχιακά s. Αλλά για άτομα που αποτελούνται από τροχιακά s και p που έχουν μη ζευγαρωμένα ηλεκτρόνια, η θεωρία του δεσμού σθένους έχει μια έννοια γνωστή ως "υβριδισμός".
Ο υβριδισμός των τροχιακών οδηγεί σε υβριδικά τροχιακά. Αυτά τα υβριδικά τροχιακά είναι διατεταγμένα με τέτοιο τρόπο ώστε η απώθηση μεταξύ αυτών των τροχιακών να ελαχιστοποιείται. Ακολουθούν ορισμένα υβριδικά τροχιακά.
sp Orbital
Αυτό το υβριδικό τροχιακό σχηματίζεται όταν ένα τροχιακό s υβριδοποιείται με ένα τροχιακό p. Επομένως, το sp τροχιακό έχει το 50% των τροχιακών χαρακτηριστικών s και το 50% των τροχιακών χαρακτηριστικών p. Ένα άτομο που αποτελείται από sp υβριδικά τροχιακά έχει δύο μη υβριδισμένα τροχιακά p. Επομένως, αυτά τα δύο τροχιακά p μπορούν να επικαλύπτονται με παράλληλο τρόπο σχηματίζοντας δύο δεσμούς pi. Η τελική διάταξη των υβριδοποιημένων τροχιακών είναι γραμμική.
spOrbital
Αυτό το υβριδικό τροχιακό σχηματίζεται από τον υβριδισμό ενός τροχιακού s με δύο τροχιακά p. Επομένως, αυτό το υβριδικό τροχιακό sp περιλαμβάνει περίπου το 33% των τροχιακών ιδιοτήτων s και περίπου το 67% των ιδιοτήτων του τροχιακού p. Τα άτομα που υφίστανται αυτόν τον τύπο υβριδισμού αποτελούνται από ένα μη υβριδοποιημένο τροχιακό p. Η τελική διάταξη του υβριδικού τροχιακού είναι τριγωνική επίπεδη.
spOrbital
Αυτό το υβριδικό τροχιακό σχηματίζεται από τον υβριδισμό ενός τροχιακού s με τρία τροχιακά p. Επομένως, αυτό το υβριδικό τροχιακό sp περιλαμβάνει περίπου το 25% των τροχιακών ιδιοτήτων s και περίπου το 75% των ιδιοτήτων του τροχιακού p. Τα άτομα που υφίστανται αυτόν τον τύπο υβριδισμού δεν έχουν μη υβριδοποιημένο τροχιακό p. Η τελική διάταξη των υβριδικών τροχιακών είναι τετραεδρική.
spdOrbital
Αυτός ο υβριδισμός περιλαμβάνει ένα τροχιακό s, τρία τροχιακά p και ένα τροχιακό d.
Αυτά τα υβριδικά τροχιακά θα καθορίσουν την τελική γεωμετρία ή το σχήμα του μορίου.

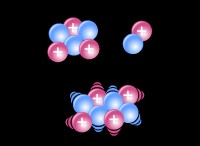
Εικόνα 1:Η γεωμετρία του CH4 είναι τετραεδρική
Η παραπάνω εικόνα δείχνει τη γεωμετρία του CH4 μόριο. Είναι τετραεδρικό. Τα χρωματισμένα τροχιακά είναι sp υβριδισμένα τροχιακά ατόμου άνθρακα, ενώ τα μπλε τροχιακά είναι τροχιακά άτομα υδρογόνου που έχουν επικαλυφθεί με υβριδικά τροχιακά ατόμου άνθρακα που σχηματίζουν ομοιοπολικούς δεσμούς.
Τι είναι η Μοριακή Τροχιακή Θεωρία
Η θεωρία των μοριακών τροχιακών εξηγεί τον χημικό δεσμό ενός μορίου χρησιμοποιώντας υποθετικά μοριακά τροχιακά. Περιγράφει επίσης πώς σχηματίζεται ένα μοριακό τροχιακό όταν τα ατομικά τροχιακά επικαλύπτονται (αναμειγνύονται). Σύμφωνα με αυτή τη θεωρία, ένα μοριακό τροχιακό μπορεί να χωρέσει το πολύ δύο ηλεκτρόνια. Αυτά τα ηλεκτρόνια έχουν αντίθετο σπιν για να ελαχιστοποιήσουν την απώθηση μεταξύ τους. Αυτά τα ηλεκτρόνια ονομάζονται ζεύγος ηλεκτρονίων δεσμού. Όπως εξηγείται σε αυτή τη θεωρία, τα μοριακά τροχιακά μπορεί να είναι δύο τύπων:μοριακά τροχιακά με δεσμό και μοριακά τροχιακά με αντισυγκόλληση.
Σύνδεση Μοριακών Τροχιακών
Τα συνδετικά μοριακά τροχιακά έχουν μικρότερη ενέργεια από τα ατομικά τροχιακά (ατομικό τροχιακό που συμμετείχε στο σχηματισμό αυτού του μοριακού τροχιακού). Επομένως, τα τροχιακά δεσμού είναι σταθερά. Τα συνδετικά μοριακά τροχιακά έχουν το σύμβολο σ.
Αντιδεσμικά Μοριακά Τροχιακά
Τα αντιδεσμικά μοριακά τροχιακά έχουν μεγαλύτερη ενέργεια από τα ατομικά τροχιακά. Επομένως, αυτά τα αντιδεσμικά τροχιακά είναι ασταθή σε σύγκριση με τα δεσμευτικά και ατομικά τροχιακά. Στα αντιδεσμικά μοριακά τροχιακά δίνεται το σύμβολο σ*.
Τα συνδεόμενα μοριακά τροχιακά προκαλούν το σχηματισμό ενός χημικού δεσμού. Αυτός ο χημικός δεσμός μπορεί να είναι είτε δεσμός σίγμα είτε δεσμός π. Τα αντιδεσμικά τροχιακά δεν εμπλέκονται στο σχηματισμό ενός χημικού δεσμού. Διαμένουν εκτός του δεσμού. Ένας δεσμός σίγμα σχηματίζεται όταν εμφανίζεται μια επικάλυψη από το κεφάλι με το κεφάλι. Σχηματίζεται ένας δεσμός pi που επικαλύπτει από μέσα σε πλευρά τροχιακά.
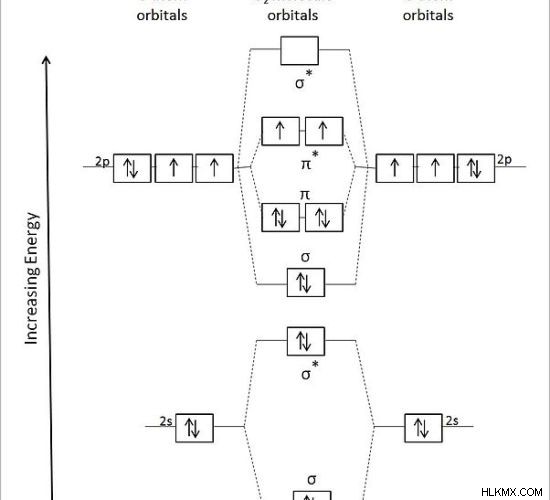
Εικόνα 2:Μοριακό τροχιακό διάγραμμα για τη σύνδεση στο μόριο οξυγόνου
Στο παραπάνω διάγραμμα, τα ατομικά τροχιακά των δύο ατόμων οξυγόνου εμφανίζονται στην αριστερή και στη δεξιά πλευρά. Στη μέση, τα μοριακά τροχιακά του O2 μόριο παρουσιάζονται ως συνδετικά και αντιδεσμικά τροχιακά.
Διαφορά μεταξύ της θεωρίας του δεσμού σθένους και της θεωρίας μοριακών τροχιακών
Ορισμός
Θεωρία δεσμού σθένους :Η θεωρία του δεσμού σθένους είναι μια βασική θεωρία που χρησιμοποιείται για να εξηγήσει τον χημικό δεσμό των ατόμων σε ένα μόριο.
Θεωρία μοριακής τροχιάς: Η θεωρία των μοριακών τροχιακών εξηγεί τον χημικό δεσμό ενός μορίου χρησιμοποιώντας υποθετικά μοριακά τροχιακά.
Μοριακά τροχιακά
Θεωρία δεσμού σθένους :Η θεωρία του δεσμού σθένους δεν δίνει λεπτομέρειες για τα μοριακά τροχιακά. Εξηγεί τη σύνδεση των ατομικών τροχιακών.
Θεωρία μοριακής τροχιάς: Η θεωρία των μοριακών τροχιακών αναπτύχθηκε με βάση τα μοριακά τροχιακά.
Τύποι τροχιακών
Θεωρία δεσμού σθένους :Η θεωρία του δεσμού σθένους περιγράφει τα υβριδικά τροχιακά.
Θεωρία μοριακής τροχιάς: Η θεωρία των μοριακών τροχιακών περιγράφει τα δεσμευτικά μοριακά τροχιακά και τα αντιδεσμικά μοριακά τροχιακά.
Υβριδισμός
Θεωρία δεσμού σθένους :Η θεωρία του δεσμού σθένους εξηγεί τον υβριδισμό των μοριακών τροχιακών.
Θεωρία Μοριακής Τροχίας: Η θεωρία των μοριακών τροχιακών δεν εξηγεί τον υβριδισμό των τροχιακών.
Συμπέρασμα
Η θεωρία του δεσμού σθένους και η θεωρία των μοριακών τροχιακών χρησιμοποιούνται για να εξηγήσουν τον χημικό δεσμό μεταξύ των ατόμων στα μόρια. Ωστόσο, η θεωρία του δεσμού σθένους δεν μπορεί να χρησιμοποιηθεί για να εξηγήσει τη σύνδεση σε πολύπλοκα μόρια. Είναι πολύ κατάλληλο για διατομικά μόρια. Αλλά η μοριακή τροχιακή θεωρία μπορεί να χρησιμοποιηθεί για να εξηγήσει τον δεσμό σε οποιοδήποτε μόριο. Ως εκ τούτου, έχει πολλές προηγμένες εφαρμογές από τη θεωρία του δεσμού σθένους. Αυτή είναι η διαφορά μεταξύ της θεωρίας του δεσμού σθένους και της θεωρίας των μοριακών τροχιακών.
Αναφορές:
1. "Εικονογραφική μοριακή τροχιακή θεωρία." LibreTexts Χημείας. Libretexts, 21 Ιουλίου 2016. Web. Διαθέσιμο εδώ. 09 Αυγούστου 2017.
2. «Θεωρία δεσμού σθένους και υβριδικά ατομικά τροχιακά». Θεωρία δεσμού σθένους και υβριδικά ατομικά τροχιακά. Ν.π., ν.δ. Ιστός. Διαθέσιμο εδώ. 09 Αυγούστου 2017.
Εικόνα Ευγενική προσφορά:
1. «Ch4 hybridization» Από τον K. Aainsqatsi στην Αγγλική Wikipedia (Αρχικό κείμενο:K. Aainsqatsi) – Δικό του έργο (Πρωτότυπο κείμενο:αυτοδημιούργητο) (Δημόσιος Τομέας) μέσω Commons Wikimedia
2. «Διάγραμμα τροχιακών μορίων οξυγόνου» Από Anthony.Sebastian – (CC BY-SA 3.0) μέσω Commons Wikimedia