Διαφορά μεταξύ Thomson και Rutherford Model of Atom
Κύρια διαφορά – Thomson vs Rutherford Model of Atom
Το μοντέλο ατόμου Thomson είναι ένα από τα παλαιότερα μοντέλα για την περιγραφή της δομής των ατόμων. Αυτό το μοντέλο είναι επίσης γνωστό ως μοντέλο πουτίγκας δαμάσκηνου λόγω της ομοιότητάς του με πουτίγκα δαμάσκηνου. Αυτό εξηγεί ότι αυτό το άτομο είναι μια σφαιρική δομή που αποτελείται από ένα θετικά φορτισμένο στερεό υλικό και τα ηλεκτρόνια είναι ενσωματωμένα σε αυτό το στερεό. Αλλά αυτό το μοντέλο απορρίφθηκε μετά την ανακάλυψη του ατομικού πυρήνα. Το μοντέλο του ατόμου του Rutherford περιγράφει τον ατομικό πυρήνα και τη θέση των ηλεκτρονίων σε ένα άτομο. Προτάθηκε ποιος περιέγραψε ότι ένα άτομο αποτελείται από έναν κεντρικό στερεό πυρήνα ο οποίος είναι θετικά φορτισμένος και τα ηλεκτρόνια βρίσκονται γύρω από αυτόν τον στερεό πυρήνα. Ωστόσο, αυτό το μοντέλο απορρίφθηκε επίσης επειδή δεν μπορούσε να εξηγήσει γιατί τα ηλεκτρόνια δεν έλκονται από τον πυρήνα. Η κύρια διαφορά μεταξύ του μοντέλου ατόμου Thomson και Rutherford είναι ότι Το μοντέλο Thomson δεν δίνει λεπτομέρειες για τον ατομικό πυρήνα, ενώ το μοντέλο Rutherford εξηγεί για τον πυρήνα.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το Thomson Model of Atom
– Ορισμός, Μοντέλο, Μειονεκτήματα
2. Τι είναι το μοντέλο Rutherford of Atom
– Ορισμός, Μοντέλο, Μειονεκτήματα
3. Ποια είναι η διαφορά μεταξύ Thomson και Rutherford Model of Atom
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Alpha Particles, Atom, Electron, Gold Foil Experiment, Nucleus, Plum Pudding Model, Rutherford Model of Atom, Thomson Model of Atom

Τι είναι το Thomson Model of Atom
Το μοντέλο ατόμου Thomson είναι η δομή ενός ατόμου που προτάθηκε από τον επιστήμονα J.J.Thomson, ο οποίος ήταν ο πρώτος άνθρωπος που ανακάλυψε το ηλεκτρόνιο. Λίγο μετά την ανακάλυψη του ηλεκτρονίου, προτάθηκε το ατομικό μοντέλο λέγοντας ότι η δομή ενός ατόμου μοιάζει με μια «πουτίγκα δαμάσκηνου».
Το μοντέλο ατόμου Thomson περιγράφεται με βάση τρία κύρια γεγονότα:
- Τα άτομα αποτελούνται από ηλεκτρόνια.
- Τα ηλεκτρόνια είναι αρνητικά φορτισμένα σωματίδια.
- Τα άτομα είναι ουδέτερα φορτισμένα.

Εικόνα 1:Μοντέλο ατόμου Thomson
Ο Thomson πρότεινε ότι εφόσον τα ηλεκτρόνια είναι αρνητικά φορτισμένα και τα άτομα είναι ουδέτερα φορτισμένα, θα πρέπει να υπάρχει θετικό φορτίο στο άτομο προκειμένου να εξουδετερωθεί το αρνητικό φορτίο των ηλεκτρονίων. Πρότεινε ότι το άτομο είναι μια στερεή, θετικά φορτισμένη, σφαιρική δομή και τα ηλεκτρόνια είναι ενσωματωμένα σε αυτή τη σφαίρα. Δεδομένου ότι αυτή η δομή μοιάζει με μια πουτίγκα με διάσπαρτα δαμάσκηνα, ονομάστηκε δομή ατόμου πουτίγκας δαμάσκηνου. Ωστόσο, αυτή η δομή απορρίφθηκε μετά την ανακάλυψη του ατομικού πυρήνα.
Μειονεκτήματα του Thomson Model of Atom
- Δεν υπάρχουν λεπτομέρειες σχετικά με τον ατομικό πυρήνα.
- Δεν υπάρχουν λεπτομέρειες σχετικά με τα ατομικά τροχιακά.
- Καμία εξήγηση σχετικά με τα πρωτόνια ή τα νετρόνια.
- Δηλώνει ότι το άτομο έχει ομοιόμορφη κατανομή μάζας, κάτι που είναι λάθος.
Τι είναι Rutherford Model of Atom
Το μοντέλο ατόμου του Rutherford περιγράφει ότι το άτομο αποτελείται από έναν ατομικό πυρήνα και ηλεκτρόνια που περιβάλλουν τον πυρήνα. Αυτό το μοντέλο προκάλεσε την απόρριψη του μοντέλου ατόμου Thomson. Το μοντέλο Rutherford προτάθηκε από τον Ernst Rutherford μετά την ανακάλυψη του ατομικού πυρήνα.
Το πείραμα με φύλλο χρυσού χρησιμοποιήθηκε από τον Rutherford για να προτείνει αυτό το ατομικό μοντέλο. Σε αυτό το πείραμα, τα σωματίδια άλφα βομβαρδίστηκαν μέσω ενός φύλλου χρυσού. αναμενόταν να περάσουν κατευθείαν μέσα από το χρυσό φύλλο. Αλλά αντί για ευθεία διείσδυση, τα σωματίδια άλφα μετατράπηκαν σε διαφορετικές κατευθύνσεις. Αυτό το πείραμα έδειξε ότι υπάρχει ένα θετικά φορτισμένο, στερεό υλικό στη μέση του ατόμου, ενώ το υπόλοιπο άτομο έχει περισσότερο κενό χώρο. Αυτός ο συμπαγής πυρήνας ονομάστηκε πυρήνας.
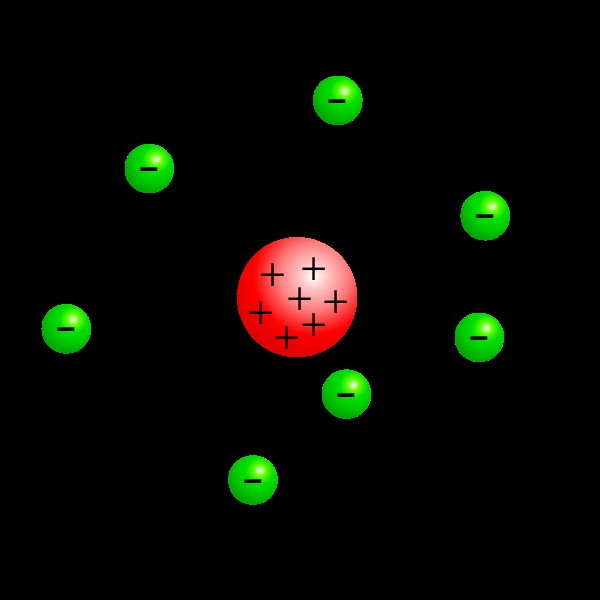
Εικόνα 2:Ατομικό μοντέλο Rutherford
Σύμφωνα με αυτό το μοντέλο,
- Το άτομο αποτελείται από ένα θετικά φορτισμένο κέντρο που ονομάζεται πυρήνας. Αυτό το κέντρο περιείχε τη μάζα του ατόμου.
- Τα ηλεκτρόνια βρίσκονται έξω από τον πυρήνα σε τροχιακά σε μεγάλη απόσταση.
- Ο αριθμός των ηλεκτρονίων είναι ίσος με τον αριθμό των θετικών φορτίων (αργότερα ονομάζονται πρωτόνια) στον πυρήνα.
- Ο όγκος του πυρήνα είναι αμελητέος σε σύγκριση με τον όγκο του ατόμου. Ως εκ τούτου, το μεγαλύτερο μέρος του χώρου στο άτομο είναι κενό.
Μειονεκτήματα του Rutherford Model of Atom
Αργότερα, το μοντέλο Rutherford απορρίφθηκε επίσης επειδή δεν μπορούσε να εξηγήσει γιατί ο θετικά φορτισμένος πυρήνας και τα ηλεκτρόνια δεν έλκονται μεταξύ τους.
Διαφορά μεταξύ Thomson και Rutherford Model of Atom
Ορισμός
Μοντέλο ατόμου Thomson :Το μοντέλο ατόμου Thomson δηλώνει ότι τα ηλεκτρόνια είναι ενσωματωμένα σε ένα θετικά φορτισμένο στερεό υλικό που έχει σφαιρικό σχήμα.
Μοντέλο ατόμου Rutherford: Το μοντέλο ατόμου Rutherford περιγράφει ότι ένα άτομο αποτελείται από έναν ατομικό πυρήνα και ηλεκτρόνια που περιβάλλουν τον πυρήνα.
Πυρήνας
Μοντέλο ατόμου Thomson :Το μοντέλο ατόμου Thomson δεν δίνει λεπτομέρειες για τον ατομικό πυρήνα.
Μοντέλο ατόμου Rutherford: Το μοντέλο του ατόμου του Rutherford εξηγεί για τον ατομικό πυρήνα.
Ηλεκτρόνια
Μοντέλο ατόμου Thomson :Το μοντέλο ατόμου Thomson δηλώνει ότι τα ηλεκτρόνια είναι ενσωματωμένα σε ένα στερεό υλικό.
Μοντέλο ατόμου Rutherford: Το μοντέλο ατόμου του Rutherford δηλώνει ότι τα ηλεκτρόνια βρίσκονται γύρω από ένα κεντρικό στερεό υλικό.
Σχήμα ατόμου
Μοντέλο ατόμου Thomson: Το μοντέλο ατόμου Thomson υποδεικνύει ότι το άτομο είναι μια σφαιρική δομή.
Μοντέλο ατόμου Rutherford: Το μοντέλο ατόμου Rutherford υποδεικνύει ότι ένα άτομο έχει έναν κεντρικό στερεό πυρήνα που περιβάλλεται από ηλεκτρόνια.
Συμπέρασμα
Το μοντέλο ατόμου Thomson και το μοντέλο ατόμου του Rutherford είναι δύο μοντέλα που προτάθηκαν από τους J.J.Thomson και Ernest Rutherford, αντίστοιχα, προκειμένου να εξηγήσουν τη δομή ενός ατόμου. Η κύρια διαφορά μεταξύ του μοντέλου ατόμου Thomson και Rutherford είναι ότι το μοντέλο Thomson δεν δίνει λεπτομέρειες για τον ατομικό πυρήνα ενώ το μοντέλο Rutherford εξηγεί για τον πυρήνα.