Ποιες είναι οι διαφορές μεταξύ μετάλλων και μη μετάλλων;
Φυσικές ιδιότητες:
* εμφάνιση: Τα μέταλλα είναι γενικά λαμπερά, λαμπερά και αδιαφανή, ενώ τα μη μέταλλα μπορεί να είναι θαμπό, εύθραυστα και διαφανή ή ημιδιαφανή.
* κατάσταση σε θερμοκρασία δωματίου: Τα περισσότερα μέταλλα είναι στερεά σε θερμοκρασία δωματίου (εκτός από τον υδράργυρο, το οποίο είναι υγρό), ενώ τα μη μέταλλα μπορεί να είναι στερεά, υγρά (όπως βρωμιά) ή αέριο (όπως το οξυγόνο).
* Μαλλιδικότητα και ολκιμότητα: Τα μέταλλα μπορούν να σφυρηλατηθούν σε λεπτές φύλλα (εύπλαστα) και να τραβηχτούν σε καλώδια (όλκιμα), ενώ τα μη μέταλλα είναι γενικά εύθραυστα και σπάζουν εύκολα.
* αγωγιμότητα: Τα μέταλλα είναι εξαιρετικοί αγωγοί θερμότητας και ηλεκτρικής ενέργειας, ενώ τα μη μέταλλα είναι κακοί αγωγοί (εκτός από τον άνθρακα με τη μορφή γραφίτη).
* Πυκνότητα: Τα μέταλλα είναι συνήθως πιο πυκνότερα από τα μη μέταλλα.
* Σημείο τήξης: Τα μέταλλα έχουν γενικά υψηλότερα σημεία τήξης από τα μη μέταλλα.
Χημικές ιδιότητες:
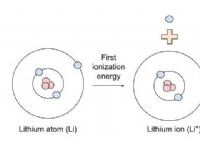
* Αντιδραστικότητα: Τα μέταλλα τείνουν να χάνουν ηλεκτρόνια για να σχηματίσουν θετικά ιόντα (κατιόντα), ενώ τα μη μέταλλα τείνουν να κερδίζουν ηλεκτρόνια για να σχηματίσουν αρνητικά ιόντα (ανιόντα).
* Οξείδωση: Τα μέταλλα εύκολα οξειδώνουν (αντιδρούν με οξυγόνο) για να σχηματίσουν οξείδια, ενώ τα μη μέταλλα μπορούν είτε να οξειδώσουν είτε να μειωθούν ανάλογα με την κατάσταση.
* Σχηματισμός ενώσεων: Τα μέταλλα συχνά αντιδρούν με μη μέταλλα για να σχηματίσουν ιοντικές ενώσεις, ενώ τα μη μέταλλα μπορούν να σχηματίσουν ομοιοπολικές ενώσεις μεταξύ τους.
Παραδείγματα:
* μέταλλα: Σίδηρος, χαλκός, χρυσός, ασήμι, αλουμίνιο, μαγνήσιο, νάτριο, κάλιο.
* Μη μετάλλια: Οξυγόνο, άζωτο, χλώριο, θείο, φωσφόρο, άνθρακας, βρωμίου, ιώδιο.
Εξαιρέσεις και ενδιαφέρουσες περιπτώσεις:
* Metalloids: Ορισμένα στοιχεία, όπως το πυρίτιο και το γερμανικό, παρουσιάζουν ιδιότητες τόσο των μετάλλων όσο και των μη μεταλλικών. Ονομάζονται μεταλλοειδή ή ημιμετρικά.
* Allotropes: Ορισμένα μη μέταλλα, όπως ο άνθρακας, μπορούν να υπάρχουν σε διαφορετικές μορφές με σημαντικά διαφορετικές ιδιότητες (π.χ. Diamond vs. Graphite).
Πίνακας συνοπτικών:
| Ιδιοκτησία | Μέταλλα | Μη μέταλλα |
| ------------------- | ---------------------------------------------------------------------------------
| Εμφάνιση | Λαμπερό, λαμπερό | Θαμπό, εύθραυστο |
| Κράτος | Στερεό (κυρίως) | Στερεό, υγρό, αέριο |
| Μεταβλαγή | Εύπλαστο | Εύθραυστο |
| Οκκύτιδα | Όλκιμο | Εύθραυστο |
| Αγωγιμότητα | Καλό | Κακή (εκτός από γραφίτη)
| Πυκνότητα | Υψηλή | Χαμηλή |
| Αντιδραστικότητα | Χάνουν ηλεκτρόνια | Κερδίστε ηλεκτρόνια |
| Οξείδωση | Οξειδώνεται εύκολα | Οξειδώνεται ή μειώνει |
| Ενώσεις | Ιωνικός | Ομοιοπολικό |
Η κατανόηση των διαφορών μεταξύ μετάλλων και μη μεταλλικών είναι ζωτικής σημασίας για την κατανόηση διαφόρων χημικών και φυσικών φαινομένων.