Πώς διαφέρει η θερμότητα του οξικού οξέος εξουδετέρωσης από αυτό το HCl ή H₂so₄;
* Οξικό οξύ (CH₃COOH) είναι ένα αδύναμο οξύ: Σε αντίθεση με τα ισχυρά οξέα όπως το HCl και το H₂so₄, το οξικό οξύ δεν ιονίζεται πλήρως σε διάλυμα. Αυτό σημαίνει μόνο ένα τμήμα των μορίων οξικού οξέος δίνουν πρωτόνια (ιόντα Η) στη βάση. Ο ελλιπής ιονισμός έχει ως αποτέλεσμα μια ασθενέστερη αλληλεπίδραση με τη βάση, οδηγώντας σε λιγότερη θερμότητα που απελευθερώνεται κατά τη διάρκεια της εξουδετέρωσης.
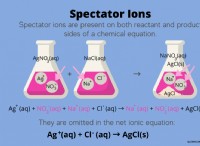
* Ισχυρά οξέα και βάσεις: Ισχυρά οξέα (HCl, H₂so₄) και ισχυρές βάσεις (όπως NaOH) εντελώς ιονίζουν σε διάλυμα. Η αντίδραση μεταξύ αυτών των ισχυρών ηλεκτρολυτών απελευθερώνει μια μεγάλη ποσότητα θερμότητας καθώς τα ιόντα Η ς από το οξύ συνδυάζονται με τα ιόντα ΟΗΑ από τη βάση για να σχηματίσουν νερό (H₂O).
Συνοπτικά:
* Ισχυρό οξύ + ισχυρή βάση: Πλήρης ιονισμός, υψηλή θερμότητα εξουδετέρωσης.
* Αδύναμο οξύ + Ισχυρή βάση: Μερικός ιονισμός, χαμηλότερη θερμότητα εξουδετέρωσης.
Παράδειγμα:
Η θερμότητα της εξουδετέρωσης των HCl και NaOH είναι περίπου -57,3 kJ/mol, ενώ η θερμότητα εξουδετέρωσης του οξικού οξέος και του ΝαΟΗ είναι περίπου -55,8 kJ/mol. Αυτή η διαφορά υπογραμμίζει τη χαμηλότερη θερμότητα που απελευθερώνεται κατά τη διάρκεια της εξουδετέρωσης ενός ασθενούς οξέος.