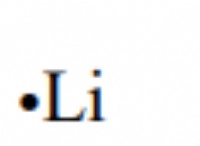Τι συμβαίνει όταν ένα ή περισσότερα ηλεκτρόνια σθένους μεταφέρονται από το άτομο σε άλλο;
1. Ηλεκτρόνια σθένους και χημικοί δεσμοί:
* Electrons Salence είναι τα ηλεκτρόνια στο εξωτερικό κέλυφος ενός ατόμου. Είναι αυτοί που εμπλέκονται στη χημική σύνδεση.
* Χημικοί δεσμοί είναι οι δυνάμεις που συγκρατούν τα άτομα μαζί σε μόρια και ενώσεις.
2. Σχηματισμός ιοντικών δεσμών:
* Όταν ένα άτομο χάνει ένα ή περισσότερα ηλεκτρόνια σθένους, γίνεται ένα θετικά φορτισμένο ιόν ( Cation ).
* Όταν ένα άτομο κερδίζει ένα ή περισσότερα ηλεκτρόνια σθένους, γίνεται ένα αρνητικά φορτισμένο ιόν ( ανιόν ).
* Τα αντίθετα φορτία του κατιόντος και του ανιόντων προσελκύουν ο ένας τον άλλον, σχηματίζοντας ένα ιονικό δεσμό .
3. Παραδείγματα:
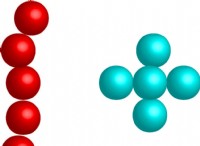
* νάτριο (Na) και χλώριο (CL): Το νάτριο έχει ένα ηλεκτρόνιο σθένους και το χλώριο έχει επτά.
* Το νάτριο χάνει το ηλεκτρόνιο σθένους του για να γίνει ιόν νατρίου (Na +), με φορτίο +1.
* Κέρδη χλωρίου που ηλεκτρόνιο για να γίνει ένα ιόν χλωριούχου (cl-), με φορτίο -1.
* Τα αντίθετα φορτία προσελκύουν, σχηματίζουν έναν ιοντικό δεσμό και δημιουργούν χλωριούχο νάτριο (NaCl) ή επιτραπέζιο αλάτι.
4. Ιδιότητες ιοντικών ενώσεων:
* Οι ιοντικές ενώσεις είναι συνήθως στερεά σε θερμοκρασία δωματίου.
* Έχουν υψηλά σημεία τήξης και βρασμού Λόγω των ισχυρών ηλεκτροστατικών δυνάμεων μεταξύ των ιόντων.
* Είναι καλοί αγωγοί ηλεκτρικής ενέργειας όταν διαλύεται σε νερό ή λιωμένο.
Συνοπτικά, η μεταφορά ηλεκτρονίων σθένους οδηγεί στο σχηματισμό ιόντων και ιοντικών δεσμών, δημιουργώντας νέες ενώσεις με ξεχωριστές φυσικές και χημικές ιδιότητες.