Γιατί είναι ο χρυσός;
Η λαμπερή κίτρινη λάμψη του χρυσού, παραδόξως, είναι η συνέπεια της θεωρίας της ειδικής σχετικότητας του Αϊνστάιν και της διπλής φύσης των ηλεκτρονίων.Για χιλιετίες, η ανθρωπότητα υπνωτίζεται από τη λαμπρότητα του μετάλλου. Διεξήχθησαν πόλεμοι, εισβολές σε ήπειρους και αποστολές οδηγήθηκαν σε πυκνές επικίνδυνες ζούγκλες, όλα για την κατοχή του αιώνιου μετάλλου - του χρυσού. Σε μια φαινομενικά άσχετη σημείωση, η θεωρία της ειδικής σχετικότητας μας λέει ότι τίποτα δεν μπορεί να ταξιδέψει πιο γρήγορα από την ταχύτητα του φωτός. Λοιπόν, περιμένετε, τι σχέση έχει η θεωρία της σχετικότητας με τον χρυσό; Λοιπόν, η θεωρία της σχετικότητας δεν είναι μόνο για φυσικούς και αστρονόμους που πρέπει να συλλογιστούν, αλλά και μια θεωρία που πρέπει να θαυμάσουμε. Μπορεί να μην το συνειδητοποιούμε, αλλά μας επηρεάζει πολύ κοντά στο σπίτι. Το λαμπερό κίτρινο χρώμα του χρυσού που έχει τυφλώσει την ανθρωπότητα με αστραφτερή απληστία είναι επίσης συνέπεια της θεωρίας της ειδικής σχετικότητας του Αϊνστάιν. Πριν ανακαλύψουμε τι κάνει το χρυσό χρυσό, πρέπει πρώτα να καταλάβουμε τι τον κάνει να λάμπει.
Γιατί τα μέταλλα είναι γυαλιστερά;
Η απλή απάντηση θα ήταν "επειδή το φως αναπηδά από την επιφάνεια", αλλά αυτό δεν ισχύει στην πραγματικότητα για τα μέταλλα. Στην περίπτωση αυτή, έχει να κάνει με μερικά πολύ μικροσκοπικά σωματίδια που χορεύουν στο ρυθμό του φωτός.Θάλασσα ηλεκτρονίων
Γνωρίζουμε καλά ότι τα μέταλλα είναι γνωστά ως εξαιρετικοί αγωγοί της θερμότητας και του ηλεκτρισμού. Αυτές οι ιδιότητες γίνονται δυνατές από χαλαρά συνδεδεμένα ηλεκτρόνια που κινούνται ελεύθερα γύρω από τον θετικά φορτισμένο πυρήνα. Όταν πολλά άτομα μετάλλων ενώνονται για να σχηματίσουν μέταλλα, δημιουργείται μια αρνητικά φορτισμένη λακκούβα ηλεκτρονίων που μπορεί να ρέει ελεύθερα. Οι επιστήμονες το αναφέρουν ως «θάλασσα ηλεκτρονίων».
Θάλασσα ηλεκτρονίων που δεν ανήκουν σε κανένα άτομο μετάλλου
Το φως, το οποίο είναι ένα ηλεκτρομαγνητικό κύμα (και μια μορφή ενέργειας), ταξιδεύει με ένα περιβάλλον - το ηλεκτρικό και μαγνητικό πεδίο (πεδίο EM). Όταν χτυπήσει οποιοδήποτε μέταλλο, τα πεδία ΗΜ δημιουργούν έναν κυματισμό στη θάλασσα των ηλεκτρονίων. Τα ηλεκτρόνια απορροφούν την ενέργεια από το φως και δονούνται με την ίδια συχνότητα φωτός που έχουν απορροφήσει. Για τα περισσότερα μέταλλα, η ενέργεια που απορροφούν αντιστοιχεί στην υπεριώδη περιοχή των κυμάτων ΗΜ. Όταν τα ηλεκτρικά φορτισμένα σωματίδια αλληλεπιδρούν μεταξύ τους, δημιουργούν ένα πεδίο. Σε αυτή την περίπτωση, η αρνητικά φορτισμένη δεξαμενή ηλεκτρονίων που κινούνται ως αποτέλεσμα του εισερχόμενου φωτός δημιουργούν ένα ηλεκτρικό πεδίο. Για να διατηρηθεί το συνολικό ηλεκτρικό πεδίο του μετάλλου μηδέν, τα ηλεκτρόνια παράγουν ένα δεύτερο κύμα φωτός (αν δεν το έκαναν, θα δεχόμασταν ένα μικροσκοπικό σοκ κάθε φορά που ακουμπούσαμε ένα γυαλιστερό μέταλλο).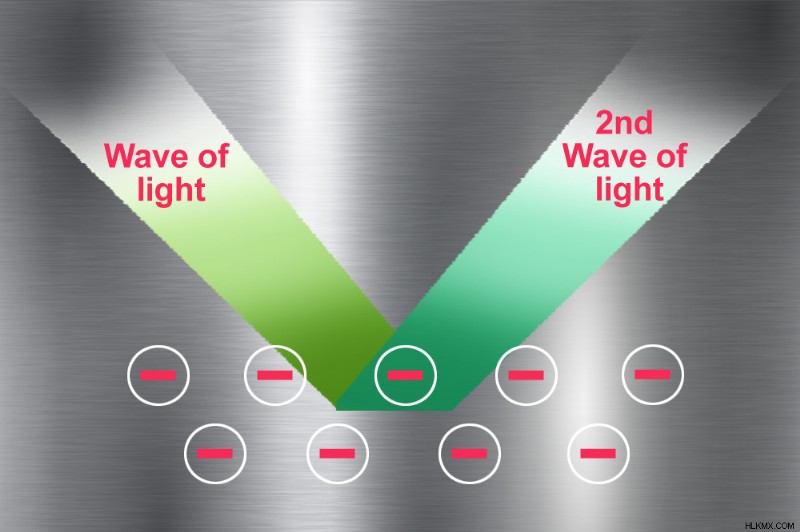
Δεύτερο κύμα φωτός που ανακλάται από τη θάλασσα ηλεκτρονίων.
Αυτό το δεύτερο κύμα φωτός που βγαίνει από το μέταλλο φτάνει στα μάτια μας και κάνει το μέταλλο να φαίνεται λαμπερό. Το φως που ανακλάται από το μέταλλο είναι ένα μείγμα μηκών κύματος όλων των χρωμάτων στην ορατή περιοχή (αν και όχι σε ίσες αναλογίες). Αυτό είναι που δίνει στα περισσότερα μέταλλα τη σχεδόν λευκή, αλλά γκριζωπή λάμψη τους… εκτός από τον αγαπημένο μας χρυσό (καθώς και τον χαλκό και το καίσιο).
Γυαλιστερές μεταλλικές σφαίρες (Photo Credit :snappygoat)
Η σχετικότητα του Αϊνστάιν και το άτομο χρυσού
Ο χρυσός είναι το 79ο στοιχείο του περιοδικού πίνακα και φέρει το σύμβολο Au . Ο πυρήνας του χρυσού αποτελείται από 79 νετρόνια και 79 πρωτόνια, καθιστώντας τον πολύ βαρύ και πυκνό. Ως εκ τούτου, το ενεργό πυρηνικό φορτίο ή το πραγματικό θετικό φορτίο που βιώνουν τα ηλεκτρόνια (επίσης 79) είναι στη συνέχεια υψηλό. Για να αποφευχθεί η πρόσκρουση στον πυρήνα λόγω ηλεκτροστατικής έλξης, τα αρνητικά φορτισμένα ηλεκτρόνια πρέπει να εργαστούν πολύ σκληρά.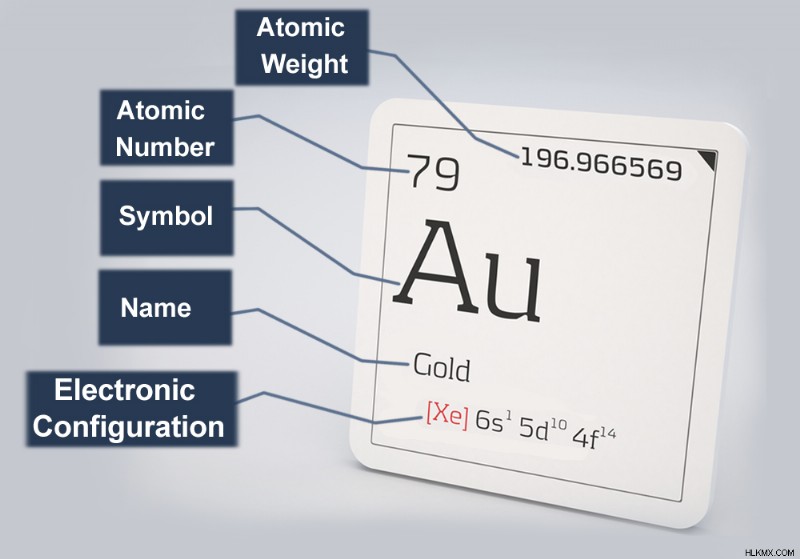
Ατομικά γεγονότα
Το ατομικό μοντέλο του Bohr
Σύμφωνα με το μοντέλο του ατόμου του Bohr, τα ηλεκτρόνια κινούνται γύρω από τον πυρήνα σε τροχιές. Διατηρούν ορισμένες ποσότητες κινητικής ενέργειας για να αποφύγουν την έλξη στον πυρήνα, παρόμοια με αυτό που θα συνέβαινε αν δέσαμε μια πέτρα σε μια κλωστή και την περιστρέψατε με μια συγκεκριμένη ταχύτητα. Θα διατηρούσε μια απόσταση από το κέντρο, αλλά τη στιγμή που θα σταματήσετε να το κάνετε αυτό, η πέτρα θα έμπαινε στο κέντρο ή θα «έπεφτε». Τα ηλεκτρόνια γύρω από τον πυρήνα του χρυσού περιστρέφονται με ταχύτητα 1,6 x 10 8 m/s (σχεδόν το ήμισυ της ταχύτητας του φωτός). Εδώ ξεκινά το σχετικιστικό φαινόμενο. Σύμφωνα με τη θεωρία της ειδικής σχετικότητας (E=mc2), όταν η ταχύτητα οποιουδήποτε σωματιδίου πλησιάζει την ταχύτητα του φωτός, αρχίζει να αποκτά μάζα. Ως αποτέλεσμα, η μάζα των ηλεκτρονίων του χρυσού αυξάνεται κατά ~20%.Ακτίνα Bohr
Αυτή η αύξηση της μάζας συρρικνώνεται στο μονοπάτι που χρειάζονται τα ηλεκτρόνια για να ταξιδέψουν γύρω από τον πυρήνα. Αυτή η «μονοπάτι» είναι επίσης γνωστή ως ακτίνα Bohr, η οποία δίνεται από τον τύπο:
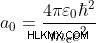 Στον τύπο, βλέπουμε ότι το a0 (ακτίνα Bohr) και το me (μάζα ενός ηλεκτρονίου) είναι αντιστρόφως ανάλογα. Αν το ένα αυξηθεί, το άλλο μειώνεται. Η μείωση της ακτίνας Bohr και η αύξηση της μάζας των ηλεκτρονίων λόγω της σχετικιστικής συστολής είναι ο λόγος που ο χρυσός λάμπει κίτρινο στα μάτια μας. Ωστόσο, μια γρήγορη ματιά στον περιοδικό πίνακα θα σας πει ότι υπάρχει μια τρύπα πλοκής σε αυτή την ιστορία. Υπάρχουν πολλά άλλα μέταλλα, όπως ο υδράργυρος και ο μόλυβδος, τα οποία είναι βαρύτερα από τον χρυσό, αλλά εξακολουθούν να έχουν ασημί λάμψη. Για να εξηγήσουμε αυτήν την φαινομενικά αντιφατική κατάσταση, χρειαζόμαστε τον σωτήρα κάθε τρύπας πλοκής της ταινίας επιστημονικής φαντασίας… Κβαντομηχανική!
Στον τύπο, βλέπουμε ότι το a0 (ακτίνα Bohr) και το me (μάζα ενός ηλεκτρονίου) είναι αντιστρόφως ανάλογα. Αν το ένα αυξηθεί, το άλλο μειώνεται. Η μείωση της ακτίνας Bohr και η αύξηση της μάζας των ηλεκτρονίων λόγω της σχετικιστικής συστολής είναι ο λόγος που ο χρυσός λάμπει κίτρινο στα μάτια μας. Ωστόσο, μια γρήγορη ματιά στον περιοδικό πίνακα θα σας πει ότι υπάρχει μια τρύπα πλοκής σε αυτή την ιστορία. Υπάρχουν πολλά άλλα μέταλλα, όπως ο υδράργυρος και ο μόλυβδος, τα οποία είναι βαρύτερα από τον χρυσό, αλλά εξακολουθούν να έχουν ασημί λάμψη. Για να εξηγήσουμε αυτήν την φαινομενικά αντιφατική κατάσταση, χρειαζόμαστε τον σωτήρα κάθε τρύπας πλοκής της ταινίας επιστημονικής φαντασίας… Κβαντομηχανική!
Το δυναμικό δίδυμο:ειδική σχετικότητα και κβαντική μηχανική
Με την εμφάνιση της κβαντικής μηχανικής, η οπτική των επιστημόνων για το «χρώμα του χρυσού» άλλαξε. Σύμφωνα με το κβαντικό μοντέλο, τα ηλεκτρόνια είναι κβαντικά σωματίδια που εμφανίζουν και κυματική και σωματιδιακή φύση και υπάρχουν σε ένα σύννεφο πιθανοτήτων. Αυτό το νέφος ηλεκτρονίων ή το ατομικό τροχιακό μας δίνει πληροφορίες σχετικά με την πιθανότητα να βρούμε ένα ηλεκτρόνιο σε μια συγκεκριμένη περιοχή στο διάστημα. Για παράδειγμα, αν ένα ηλεκτρόνιο βρισκόταν σε ένα ποδήλατο, το μοντέλο του Bohr θα περιόριζε τη διαδρομή σε έναν δρόμο, ενώ το κβαντικό μοντέλο θα το άφηνε να οδηγεί οπουδήποτε σε έναν συγκεκριμένο ταχυδρομικό κώδικα.
Διαφορετικά σχήματα νεφών ηλεκτρονίων γύρω από τον πυρήνα (Photo Credit :ThreePhaseAC
/Wikimedia Commons)

Σχήμα ατομικού τροχιακού του s τροχιακού (Πιστωτική φωτογραφία :Geek3/Wikimedia Commons)
Ως αποτέλεσμα, όλα τα τροχιακά s σε ένα άτομο χρυσού έλκονται ελαφρώς πιο κοντά στον πυρήνα. Το εξώτατο τροχιακό του χρυσού, που είναι 6s, συστέλλεται κατά ~17%. Ο συνωστισμός των τροχιακών s προς τον πυρήνα μειώνει την αποτελεσματική έλξη που βιώνουν άλλα τροχιακά που διαστέλλονται μακριά από τον πυρήνα. Αυτό μειώνει την απόσταση μεταξύ του τελευταίου τροχιακού (6s) και του δεύτερου έως του τελευταίου τροχιακού (5d).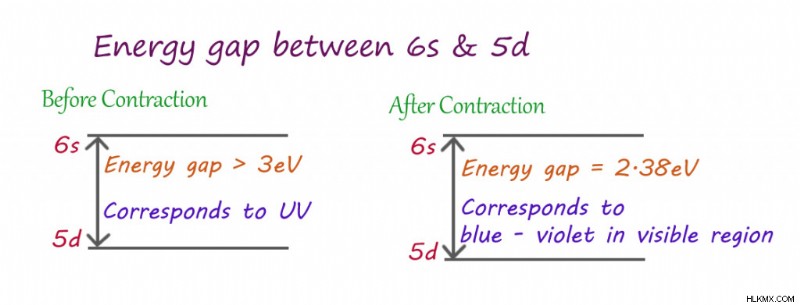
Επίδραση σχετικιστικής συστολής
Όπως διαπιστώθηκε νωρίτερα, όταν το φως πέφτει πάνω σε χρυσό, η θάλασσα των ηλεκτρονίων απορροφά αυτή την ενέργεια. Τα άτομα χρυσού απορροφούν την ακριβή ποσότητα ενέργειας που απαιτείται για να μεταπηδήσουν από το τροχιακό 5d χαμηλότερης ενέργειας στο τροχιακό 6s υψηλότερης ενέργειας. Δεδομένου ότι τα 5d και 6s είναι πιο κοντά, λόγω της σχετικιστικής συστολής, τα ηλεκτρόνια απορροφούν λιγότερη ενέργεια για τέτοιες μεταβάσεις από το συνηθισμένο. Η ενέργεια που απορροφάται από τα άτομα χρυσού ανήκει στην μπλε-ιώδες περιοχή του ορατού φάσματος (αντί της υπεριώδους περιοχής). Το δεύτερο κύμα που ανακλάται από το μέταλλο αποτελείται από όλα τα άλλα χρώματα του ορατού φάσματος, εκτός από τα μπλε και τα βιολέ. Τα ορατά μήκη κύματος φωτός που φτάνουν στα μάτια μας ανήκουν στην κόκκινη-πράσινη περιοχή και όταν αυτά συνδυάζονται, μας δίνουν Κίτρινο!Συμπέρασμα
Η επίδραση του E=mc2 στον χρυσό δεν τελειώνει μόνο με την έκθαμψή του. Επίσης, εμποδίζει τον χρυσό να αντιδρά με περιβαλλοντικούς παράγοντες, διατηρώντας τον άψογο για όλη την αιωνιότητα. Η ικανότητα του χρυσού να αφήνει το ορατό φως και να αντανακλά τις υπεριώδεις ακτίνες και τις υπέρυθρες ακτίνες τον έχει κάνει αναπόσπαστο μέρος του σχεδιασμού διαστημικών στολών (για παράδειγμα, των προσωπίδων). Είναι επίσης κρίσιμο σε δορυφορικά εξαρτήματα λόγω της μεγάλης ηλεκτρικής αγωγιμότητας και της ατρωσίας του έναντι της διάβρωσης από τις υπεριώδεις ακτίνες και τις ακτίνες Χ.
Έτσι, την επόμενη φορά που κάποιος θα πει "Η θεωρία της ειδικής σχετικότητας δεν επηρεάζει την καθημερινή ζωή", απλώς υπενθυμίστε του ότι διατηρεί τα κοσμήματά μας λαμπερά και τα συστήματα GPS μας λειτουργούν.

Ένα λεπτό στρώμα χρυσού είναι επικαλυμμένο στις προσωπίδες των αστροναυτών (Φωτογραφία :MGS/Shutterstock)