Πώς σχηματίζονται οι ομοιοπολικοί δεσμοί
Η ιδέα του χημικού δεσμού προτάθηκε για πρώτη φορά το 1916 από τους W. Kossel και G.N. Λουδοβίκος. Βρήκαν ότι όλα τα ευγενή αέρια διατηρούν οκτώ ηλεκτρόνια στο εξωτερικό τους περίβλημα με εξαίρεση το ήλιο, όπου μόνο δύο ηλεκτρόνια υπάρχουν στο εξωτερικό περίβλημα. Πρότειναν επίσης όλα τα άλλα στοιχεία να προσπαθήσουν να επιτύχουν τη διαμόρφωση των ευγενών αερίων χάνοντας, κερδίζοντας ή μοιράζοντας ηλεκτρόνια όταν σχηματίζουν ενώσεις. Αυτή ήταν η βάση για τις πρώτες έννοιες για το πώς σχηματίζονται οι χημικοί δεσμοί.
Αυτό το άρθρο εξετάζει,
1. Τι είναι οι διαφορετικοί τύποι χημικών δεσμών
– Ιωνικός δεσμός
– Ομοιοπολικός δεσμός
– Metallic Bond
2. Πώς σχηματίζονται οι ομοιοπολικοί δεσμοί
Τι είναι οι διαφορετικοί τύποι χημικών δεσμών
Υπάρχουν τρεις κύριοι τύποι χημικών δεσμών:ιονικοί, ομοιοπολικοί, μεταλλικοί. Ο τύπος του δεσμού εξαρτάται από τον αριθμό των ηλεκτρονίων και τη διάταξη των ηλεκτρονίων στις τροχιές των ατόμων. Επιπλέον, υπάρχει ένας διαφορετικός τύπος δεσμού που ονομάζεται διαμοριακοί δεσμοί, ο οποίος περιλαμβάνει δεσμούς υδρογόνου, δεσμούς διπολικού δεσμού και δεσμούς διασποράς.
Ιωνικοί δεσμοί συμβαίνουν όταν τα άτομα μετάλλων δίνουν ηλεκτρόνια σε άτομα μη μετάλλου. Έτσι, εμφανίζονται ιονικοί δεσμοί μεταξύ μετάλλων και μη μετάλλων (π.χ. χλωριούχο νάτριο).
Ομοιοπολικοί δεσμοί προκύπτουν μέσω της κατανομής του ηλεκτρονίου σθένους μεταξύ δύο ατόμων.
Μεταλλικοί δεσμοί είναι αρκετά παρόμοιοι με τους ομοιοπολικούς δεσμούς καθώς μοιράζονται ηλεκτρόνια μεταξύ των ατόμων. Αλλά σε αντίθεση με τους ομοιοπολικούς δεσμούς, τα ηλεκτρόνια σθένους που συγκρατούν τα άτομα μαζί κινούνται ελεύθερα μέσα στο μεταλλικό πλέγμα.
Τώρα, ας δούμε πώς σχηματίζονται οι ομοιοπολικοί δεσμοί.
Πώς σχηματίζονται οι ομοιοπολικοί δεσμοί
Ένας ομοιοπολικός δεσμός προκύπτει όταν δύο άτομα μη μετάλλου μοιράζονται τα ηλεκτρόνια τους για να επιτύχουν τη διαμόρφωση ηλεκτρονίων ευγενούς αερίου. Αντί να δίνει ή να λαμβάνει ηλεκτρόνια, κάθε άτομο θα μοιράζεται ηλεκτρόνια επικαλύπτοντας την εξωτερική του περιφέρεια. Αυτά τα κοινά ηλεκτρόνια ονομάζονται ηλεκτρόνια σθένους. Οι ταυτόχρονες δυνάμεις μεταξύ δύο θετικά φορτισμένων πυρήνων προς κοινά ηλεκτρόνια κρατούν και τα δύο άτομα μαζί. Μονοί, διπλοί και τριπλοί δεσμοί φαίνονται μόνο στις ομοιοπολικές ενώσεις. Ένας απλός ομοιοπολικός δεσμός εμφανίζεται όταν εμπλέκεται ένα μόνο ζεύγος ηλεκτρονίων. Σε αυτή την περίπτωση, κάθε άτομο μοιράζεται ένα μόνο ηλεκτρόνιο. Ένας διπλός δεσμός προκύπτει όταν εμπλέκονται δύο ζεύγη ηλεκτρονίων. Σε αυτή την περίπτωση, κάθε άτομο παρέχει δύο ηλεκτρόνια για τον δεσμό. Όταν σχηματίζεται ένας τριπλός δεσμός, εμπλέκονται τρία ζεύγη ηλεκτρονίων. Σε τριπλούς δεσμούς, κάθε άτομο μοιράζεται τρία ηλεκτρόνια στο εξωτερικό του περίβλημα. Τα μόρια που σχηματίζονται από ομοιοπολικούς δεσμούς ονομάζονται ομοιοπολικά μόρια. 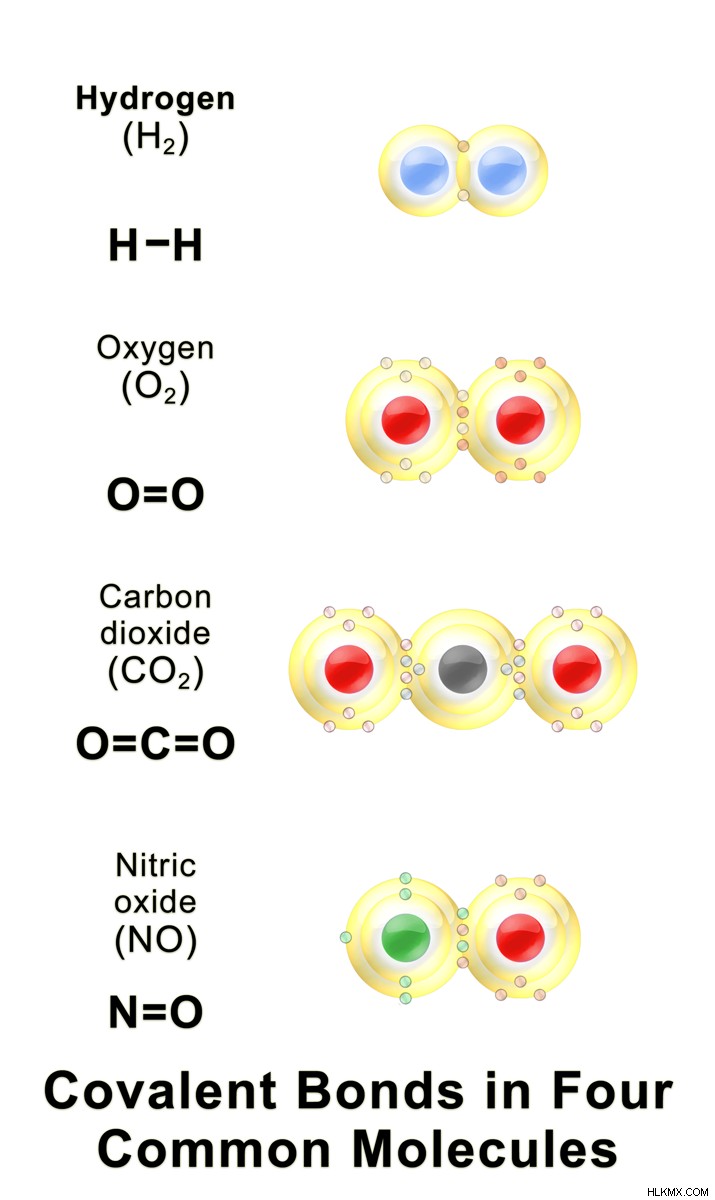
Οι ομοιοπολικές ενώσεις έχουν πολλές παρόμοιες ιδιότητες αφού μοιράζονται ηλεκτρόνια. Όλα τα ομοιοπολικά στερεά μπορούν να κατηγοριοποιηθούν σε δύο κατηγορίες:κρυσταλλικά στερεά και άμορφα στερεά. Τα κρυσταλλικά στερεά είναι σκληρά υλικά. Το διαμάντι είναι ένα παράδειγμα κρυσταλλικού στερεού και είναι το σκληρότερο υλικό στη γη. Τα άμορφα στερεά δεν είναι πολύ σκληρά. Σε ομοιοπολικές ουσίες, ο ηλεκτρισμός δεν μπορεί να μεταφερθεί λόγω έλλειψης ελεύθερων ηλεκτρονίων. Έτσι, οι ομοιοπολικές ενώσεις είναι γνωστό ότι είναι καλοί μονωτές. Μερικά κοινά παραδείγματα ομοιοπολικών ενώσεων περιλαμβάνουν αέριο υδρογόνο, αέριο οξυγόνο, αέριο διοξείδιο του άνθρακα, μεθάνιο, διοξείδιο του πυριτίου, διαμάντια κ.λπ.
Αναφορά:
Μπάρτον, Τζορτζ. Chemical Ideas – Salters advanced chemistry . Τομ. 4. Ν.π.:Heinemann, 2000. Εκτύπωση.Γουέστ, Κρίστα. Τα βασικά των χημικών αντιδράσεων . N.p.:The Rosen Publishing Group, 2013. Εκτύπωση.
Μάγιερς, Ρίτσαρντ. Τα Βασικά της Χημείας . N.p.:Greenwood Publishing Group, 2003. Εκτύπωση.



