Διαφορά μεταξύ U 235 και U 238
Κύρια διαφορά – U 235 vs U 238
Τα ραδιενεργά στοιχεία είναι ενώσεις που διασπώνται με την πάροδο του χρόνου απελευθερώνοντας ενέργεια και μετατρέπονται σε διαφορετικά στοιχεία. Αυτό συμβαίνει επειδή αυτά τα στοιχεία δεν είναι σταθερά. Προκειμένου να γίνουν σταθερά, απελευθερώνουν ενέργεια μέσω της ραδιενεργής διάσπασης. Σχεδόν όλα τα στοιχεία βρίσκονται σε διάφορες μορφές γνωστές ως ισότοπα. Μερικά από αυτά τα ισότοπα είναι πολύ σταθερά στη φύση τους. Αλλά άλλα ισότοπα δεν είναι σταθερά και υφίστανται ραδιενεργό διάσπαση. Αυτά τα ισότοπα ονομάζονται ραδιενεργά ισότοπα. Ωστόσο, ακόμη και σταθερά ισότοπα μπορεί να υποστούν ραδιενεργό διάσπαση, αλλά δεν μπορεί να παρατηρηθεί καθώς αυτή η διαδικασία διαρκεί πολύ χρόνο. Το ουράνιο είναι ένα χημικό στοιχείο γνωστό για τη ραδιενεργή αποσύνθεσή του. Τα U-235 και U-238 είναι δύο ραδιενεργά ισότοπα του Ουρανίου. Η κύρια διαφορά μεταξύ U-235 και U-238 είναι ότι ο αριθμός των νετρονίων που υπάρχουν στον πυρήνα U-235 είναι 143 ενώ ο αριθμός των πρωτονίων που υπάρχουν στον πυρήνα U-238 είναι 146.
Βασικές περιοχές που καλύπτονται
1. Τι είναι το U 235
– Ορισμός, ιδιότητες και χρήσεις
2. Τι είναι το U 238
– Ορισμός, ιδιότητες και χρήσεις
3. Ποιες είναι οι ομοιότητες μεταξύ U 235 και U 238
– Περίληψη κοινών χαρακτηριστικών
4. Ποια είναι η διαφορά μεταξύ U 235 και U 238
– Σύγκριση βασικών διαφορών
Βασικοί όροι:Half-Life, Ισότοπο, Νετρόνια, Πρωτόνια, Ραδιενεργή Διάσπαση, Ουράνιο
Τι είναι το U 235
Το U-235 είναι ένα ισότοπο του χημικού στοιχείου Ουράνιο που αποτελείται από 92 πρωτόνια και 143 νετρόνια στον πυρήνα του. Το χημικό σύμβολο για το Ουράνιο δίνεται ως 92 U. Η φυσική αφθονία του U-235 είναι περίπου 0,72%. Η μάζα αυτού του ισοτόπου είναι περίπου 235.043 amu.
Ο χρόνος ημιζωής ενός ισοτόπου U-235 βρέθηκε ότι είναι περίπου 700 εκατομμύρια χρόνια. Με άλλα λόγια, χρειάζονται περίπου 700 εκατομμύρια χρόνια για να φτάσει το ήμισυ της μάζας του μέσω της ραδιενεργής διάσπασης. Ο τρόπος αποσύνθεσης που μπορεί να δει κανείς στο U-235 είναι η διάσπαση άλφα. Αυτό σημαίνει ότι το U-235 απελευθερώνει ένα σωματίδιο άλφα όταν υφίσταται ραδιενεργό διάσπαση.
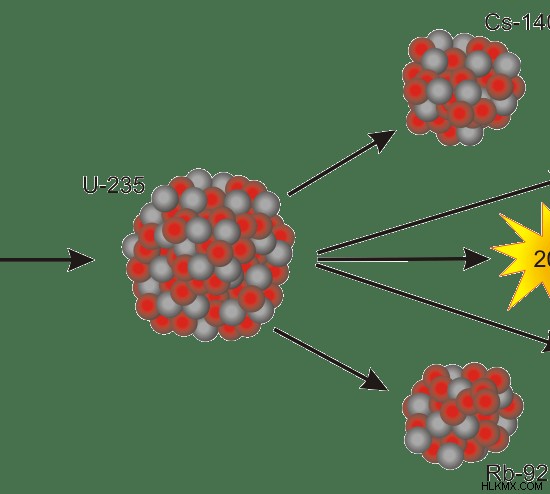
Εικόνα 1:Η αλυσιδωτή αντίδραση της σχάσης του U-235 μπορεί να ξεκινήσει με τον βομβαρδισμό ενός νετρονίου υψηλής ταχύτητας.
Το U-235 είναι ικανό να διατηρήσει μια αλυσιδωτή αντίδραση πυρηνικής σχάσης. Επομένως το U-235 είναι σχάσιμο. Μια φυσική αλυσίδα σχάσης θα τελειώσει με το Θόριο-231, το οποίο είναι ένα σταθερό στοιχείο. Η σχάση ενός ατόμου U-235 απελευθερώνει 202,5 MeV. Οι κύριες χρήσεις του U-235 περιλαμβάνουν εφαρμογές σε πυρηνικά όπλα και πυρηνικούς σταθμούς.
Τι είναι το U 238
Το U-238 είναι ένα ισότοπο του Ουρανίου, το οποίο αποτελείται από 92 πρωτόνια και 146 νετρόνια στον πυρήνα του. Είναι το πιο άφθονο ισότοπο στοιχείου ουρανίου. Η αφθονία του U-238 είναι περίπου 99%. Είναι μη σχάσιμο, που σημαίνει ότι το U-238 δεν υφίσταται καμία αλυσιδωτή αντίδραση πυρηνικής σχάσης.
Ωστόσο, μπορούν να γίνουν σχάσιμα με βομβαρδισμό ενός νετρονίου υψηλής ταχύτητας. Ως εκ τούτου, ονομάζεται γόνιμο υλικό. Αλλά ακόμη και με αυτόν τον βομβαρδισμό, η πιθανότητα να γίνει σχάσιμος είναι πολύ μικρή. Όταν ο πυρήνας πιάνει ένα νετρόνιο, σχηματίζει ασταθές ισότοπο U-239. Αυτό το ισότοπο U-239 είναι σχάσιμο και ξεκινά μια αλυσιδωτή αντίδραση ραδιενεργής αποσύνθεσης.

Εικόνα 2:Ουράνιο-238
Ο χρόνος ημιζωής του U-238 είναι περίπου 4,4 δισεκατομμύρια χρόνια. Η μοριακή μάζα αυτού του ισοτόπου είναι περίπου 238,05 amu. Αυτό το ισότοπο τείνει επίσης σε διάσπαση άλφα. Το τελικό προϊόν αυτής της διάσπασης είναι το Θόριο-234.
Τα σύγχρονα πυρηνικά όπλα χρησιμοποιούν το U-238 ως υλικό παραβίασης. Καλύπτει τον πυρήνα που περιέχει σχάσιμο υλικό. Είναι χρήσιμο στην ανάκλαση των νετρονίων που απελευθερώνονται και αυξάνει την αποτελεσματικότητα του όπλου.
Similarities Between U 235 and U 238">Similarities Between U 235 and U 238
- Το U 235 και το U 238 είναι ισότοπα του ίδιου χημικού στοιχείου. Ουράνιο.
- Και τα δύο είναι ραδιενεργά ισότοπα.
- Και τα δύο ισότοπα αποτελούνται από 92 πρωτόνια στον πυρήνα τους.
- Και τα δύο χρησιμοποιούνται στην παραγωγή πυρηνικών όπλων.
- Και οι δύο τύποι υφίστανται αποσύνθεση άλφα.
Διαφορά μεταξύ U 235 και U 238
Ορισμός
U 235: Το U-235 είναι ένα ισότοπο του Ουρανίου και αποτελείται από 92 πρωτόνια και 143 νετρόνια στον πυρήνα του.
U 238: Το U-238 είναι ένα ισότοπο του Ουρανίου και αποτελείται από 92 πρωτόνια και 146 νετρόνια στον πυρήνα του.
Νετρόνια
U 235: Ο αριθμός των νετρονίων που υπάρχουν στον πυρήνα U-235 είναι 143.
U 238: Ο αριθμός των νετρονίων που υπάρχουν στον πυρήνα U-238 είναι 146.
Χρόνος ημιζωής
U 235: Ο χρόνος ημιζωής του U-235 είναι περίπου 703 εκατομμύρια χρόνια.
U 238: Ο χρόνος ημιζωής του U-238 είναι περίπου 4,4 δισεκατομμύρια χρόνια.
Αφθονία
U 235: Η φυσική αφθονία του U-235 είναι περίπου 0,72%.
U 238: Η φυσική αφθονία του U-238 είναι περίπου 99%.
Κατηγορία
U 235: Το U-235 είναι σχάσιμο υλικό.
U 238: Το U-238 είναι ένα γόνιμο υλικό.
Αλυσιακές αντιδράσεις
U 235: Το U-235 είναι ικανό να συντηρεί αλυσιδωτές αντιδράσεις πυρηνικής σχάσης.
U 238: Το U-238 από μόνο του δεν είναι ικανό να διατηρήσει αλυσιδωτές αντιδράσεις πυρηνικής σχάσης.
Ατομική μάζα
U 235: Η μάζα του ατόμου U-235 είναι περίπου 235.043 amu.
U 238: Η μάζα του ατόμου U-238 είναι περίπου 238,05 amu.
Συμπέρασμα
Το ουράνιο είναι ένα πολύ γνωστό ραδιενεργό υλικό. Έχει πολλά ισότοπα και όλα αυτά τα ισότοπα είναι ραδιενεργά στη φύση. Τα U-235 και U-238 είναι τέτοια ισότοπα του Ουρανίου. Η κύρια διαφορά μεταξύ U-235 και U-238 είναι ότι ο αριθμός των νετρονίων που υπάρχουν στον πυρήνα U-235 είναι 143 ενώ ο αριθμός των πρωτονίων που υπάρχουν στον πυρήνα U-238 είναι 146.