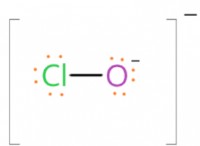Ποιο χαρακτηριστικό των ατόμων τους επιτρέπει να συνδέονται με άλλες ενώσεις μορφής;
Εδώ είναι γιατί:
* ηλεκτρόνια σθένους: Αυτά είναι τα ηλεκτρόνια στο εξωτερικό επίπεδο ενέργειας ενός ατόμου. Είναι αυτοί που εμπλέκονται στη χημική σύνδεση.
* επιθυμία για σταθερότητα: Τα άτομα είναι πιο σταθερά όταν έχουν ένα πλήρες εξωτερικό κέλυφος ηλεκτρονίων. Αυτό συχνά αναφέρεται ως ο "κανόνας οκτάδων" (8 ηλεκτρόνια), αν και υπάρχουν εξαιρέσεις.
* συγκόλληση για την επίτευξη σταθερότητας: Για να επιτευχθεί ένα πλήρες εξωτερικό κέλυφος, τα άτομα μπορούν είτε να κερδίσουν, να χάσουν είτε να μοιραστούν ηλεκτρόνια σθένους. Αυτή η κοινή χρήση ή η μεταφορά ηλεκτρονίων αποτελεί τη βάση των χημικών δεσμών.
Τύποι ομολόγων:
* Ιονικά ομόλογα: Σχηματίζεται όταν ένα άτομο μεταφέρει ηλεκτρόνια σε ένα άλλο, δημιουργώντας αντίθετα φορτισμένα ιόντα που προσελκύουν ο ένας τον άλλον.
* ομοιοπολικοί δεσμοί: Σχηματίζονται όταν τα άτομα μοιράζονται ηλεκτρόνια για να επιτύχουν ένα πλήρες εξωτερικό κέλυφος.
Συνοπτικά, ο δεσμός των ατόμων για την επίτευξη της σταθερότητας χειρίζοντας τα ηλεκτρόνια σθένους τους μέσω διαφορετικών τύπων δεσμών.